Terapeutiese argief nr. 03 2018 - Hemochromatosis - die huidige toestand van die probleem

Hemochromatosis is 'n oorerflike patologie wat verband hou met 'n hoë opname van yster in die spysverteringsorgane en die daaropvolgende oormatige opeenhoping in verskillende interne organe.
Die lewer ly meer as ander. Die vroeë opsporing van hemochromatose, die diagnose en behandeling daarvan, laat die gevolge nie toe nie.
Hemochromatosis - moderne toestand van die probleem
N.B. VOLOSHINА1, M.F. OSIPENKO1, N.V. LITVINOVA1, A.N.VOLOSHIN2
1 Novosibirsk State Medical University FGBOU in die NSMU van die Ministerie van Gesondheid van Rusland, Rusland,
2Novosibirsk City Clinical Hospital 2, Rusland
Die ysteroorlading-sindroom kan geassosieer word met verskillende verworwe toestande en oorerflike faktore. Erflike hemochromatose is die algemeenste genetiese afwyking. Sonder terapeutiese ingryping kan die siekte lei tot die ontwikkeling van lewensgevaarlike komplikasies soos sirrose, hepatosellulêre karsinoom. Die artikel bevat inligting oor patogenese, diagnose en behandeling van oorerflike hemochromatose. Eie kliniese waarneming word gegee.
sleutelwoorde: oorerflike hemochromatose, behandeling, flebotomie.
 Hemochromatosis is 'n siekte wat verband hou met die ophoping van hoë patologiese vlakke van yster in die liggaam, wat lei tot funksionele afwykings van sommige organe. Tipies word die opname van yster streng gereguleer, waardeur die liggaam nie die oortollige yster kan afskei nie. Oormatige yster versamel in die selle as hemosiderien. Dit lei uiteindelik tot seldood en die vervanging van hierdie selle met veselagtige weefsel, wat lei tot ontwrigting van die struktuur en funksie van organe. Met hemochromatose is skade aan die lewer, pankreas, hart, skildklier, gewrigte, vel, gonades en pituïtêre klier moontlik.
Hemochromatosis is 'n siekte wat verband hou met die ophoping van hoë patologiese vlakke van yster in die liggaam, wat lei tot funksionele afwykings van sommige organe. Tipies word die opname van yster streng gereguleer, waardeur die liggaam nie die oortollige yster kan afskei nie. Oormatige yster versamel in die selle as hemosiderien. Dit lei uiteindelik tot seldood en die vervanging van hierdie selle met veselagtige weefsel, wat lei tot ontwrigting van die struktuur en funksie van organe. Met hemochromatose is skade aan die lewer, pankreas, hart, skildklier, gewrigte, vel, gonades en pituïtêre klier moontlik.
Ysteroorlading, wat hemochromatose veroorsaak, kan op drie maniere voorkom: massiewe orale ysterinname, verhoogde ysteropname tydens normale ysterinname, en oormatige produksie of massiewe, gereelde oortapping van rooibloedselle.
By oorerflike hemochromatose word oortollige yster gewoonlik in parenchymale selle neergesit, terwyl dit by transfusie-hemochromatose hoofsaaklik in retikulo-endoteliale selle 1-3 gestort word.
Erflike hemochromatose bevat 'n groep genetiese afwykings wat gekenmerk word deur 'n verhoogde opname van yster. Die oorheersende meganisme in die meeste soorte oorerflike hemochromatose is die hepcidien-effek, wat 'n sleutelrol speel in yster-homeostase 4-6. Hepcidin word hoofsaaklik in hepatosiete gesintetiseer en beheer die konsentrasie van yster in plasma deur te bind aan ferroportien (ook SLC40A1 genoem), die enigste bekende transmembraantransporteur van yster uit ysterskenkersweefsel. Ferroportin voer yster uit die duodenum, van makrofage en hepatosiete uit.
In plasma bind yster aan trasferrin, dus is die ysterversadiging met transferrin gemiddeld 35% (gemiddelde oggendwaarde). Hepsidien belemmer die vrystelling van yster vanaf makrofage (van ou rooibloedselle en ferritien), hepatosiete en duodenale enterosiete deur te bind aan ferroportien. En in die afwesigheid van ferroportien, word die produksie van yster vanaf enterosiete, hepatosiete en makrofage geblokkeer. Dus verminder hepcidien die absorpsie van yster in die ingewande, verlaag die vlak van vrygestelde yster uit hepatosiete en makrofage, wat lei tot 'n lae vlak van yster in plasma en 'n toename in weefsel.
Die oorsaak van oorerflike hemochromatose is 'n mutasie in die HFE-geen. Die defek in die HFE-geen is in 1996 die eerste keer beskryf, wat 'n mutasie is wat lei tot die vervanging van tyrosien met cysteïen in die aminosuurposisie 282 (C282Y). 'N Mutasie in die HFE-geen veroorsaak verhoogde opname van yster, ondanks normale ysterinname. Die HFE-proteïen reguleer die produksie van hepcidien. Pasiënte met oorerflike hemochromatose homosigote C282Y is van 80 tot 85% 1, 8.
Daar is nog twee mutasies: een hou verband met die vervanging van aspartaat met histidien op posisie 63 (H63D), en die tweede is die vervanging van cysteïne met serien in posisie 65 (S65C). Hierdie mutasies hou nie verband met die ysteroorlading-sindroom nie, tensy C282Y 'n integrale deel van die C282Y / H63D of C282Y / S65C-heterosigos is. Die HFE-geassosieerde vorm van oorerflike hemochromatose kan dus met 'n asimptomatiese verloop van die siekte geverifieer word. Gevolglik kan 'n genetiese diagnose toegepas word by pasiënte by wie hemochromatose nog nie fenotipies gemanifesteer het nie. Hierdie groep pasiënte met 'n genetiese geneigdheid tot hemochromatose. Heterozygote het 'n verhoogde risiko vir die ontwikkeling van diabetes in vergelyking met die algemene bevolking, en die meganisme van ontwikkeling is onbekend 9-11.
Daar is voorheen gedink dat by alle pasiënte met 'n HFE-geenafwyking 'n hemochromatose-kliniek mettertyd sal ontwikkel. Daar is egter nou gevind dat fenotipiese uitdrukking slegs by ongeveer 70% van die homosigote van C282Y aangetref word, en dat minder as 10% van hulle ernstige ysteroorlading opdoen met skade aan interne organe 12, 13.
Die tabel toon die indeling van ysteroorladsindrome, afhangende van die oorsaak van die voorkoms daarvan.
Afhangend van die oorsaak van die siekte, kan pasiënte met 'n ysteroorlading-sindroom in 4 groepe verdeel word: pasiënte met oorerflike hemochromatose, pasiënte met sekondêre hemochromatose wat deur verskillende oorsake veroorsaak word, en 'n klein groepie pasiënte wat uitstaan as 'anders'.
Die oorsaak van sekondêre hemochromatose is eritropoëtiese hemochromatose. Dit kom meestal voor as gevolg van 'n onderliggende bloedsiekte waarin rooibloedselle 'n korter lewensduur het. Hierdie groep siektes sluit in ystertekortanemie, thalassemie, sideroblastiese anemie, chroniese hemolitiese anemie, aplastiese anemie, piridoksien-sensitiewe anemie, pirovaat kinase tekort.
Ysteroorlading-sindroom kan voorkom by pasiënte wat langdurige en veelvuldige oortappings van rooibloedselle ontvang. Soos uit die tabel gesien kan word, kan ander taamlik seldsame siektes, soos byvoorbeeld porfirie, ook ysterversorgingsindroom veroorsaak.
Laastens kan oormatige inname van yster hemochromatose veroorsaak. Bekende historiese feit: die gebruik van bier wat in staalvate gemaak is, was die oorsaak van ysteroorlading-sindroom. 'N Oordosis ysterpreparate kan ook 'n ysteroorlading sindroom veroorsaak. Daar moet onthou word dat baie aanvullende voedingsaanvullings yster in 'n voldoende groot dosis bevat, sodat die onbeheerde gebruik daarvan onaanvaarbaar is.
Simptome van die siekte is afhanklik van die orgaan wat die meeste geraak word, maar bykans alle pasiënte kla van beduidende swakheid en moegheid. Daar is geen spesifieke simptome van hemochromatose nie. Die diagnose word meestal gemaak op die stadium van die siekte, toe verskeie stelsels reeds geraak is. Van die eerste simptome van die siekte tot die verifiëring van die diagnose duur gewoonlik minstens tien jaar. By vroue met hemochromatose manifesteer die simptome van die siekte op 'n latere ouderdom as by mans as gevolg van die verlies van menstruele bloed, die verlies van 'moederlike yster' tydens swangerskap en die antioksidant-effek van estrogeen, en die siekte manifesteer hom nie klinies voor die klimakteriese periode nie.
Ongeveer 50% van die pasiënte met simptome van oorerflike hemochromatose het diabetes mellitus, die risiko vir die voorkoms daarvan neem aansienlik toe in heterosigote. Lewersirrose is teenwoordig by 70% van die pasiënte met hemochromatose. In hierdie groep pasiënte word die voorkoms van hepatosellulêre karsinoom, wat die grootste oorsaak van dood is, aansienlik verhoog.
Skade aan gewrigte met hemochromatose manifesteer in die vorm van artralgie (gewoonlik die tweede en derde metakarpofangeale gewrigte). Gesamentlike misvormings met hemochromatose kom gewoonlik nie voor nie, hoewel degeneratiewe gewrigsveranderings moontlik is. By hierdie pasiënte kan daar gewoonlik kristalle van kalsiumpyrofosfaat in die sinoviale vloeistof gevind word. Dit is kenmerkend van polartritis met hemochromatose dat dit selfs na normalisering van ystervoorrade steeds kan vorder.
Afsetting van yster in die vesels van die hartspier en selle van die geleidingstelsel van die hart kan lei tot versteuring van die hartritme en / of verwaterde kardiomiopatie, met die verdere ontwikkeling van hartversaking. In sommige gevalle is daar 'n volledige vergoeding vir die mislukking van die linker ventrikel nadat die ystervlak 9-12 normaliseer is.
Met hemochromatose is die ontwikkeling van hipogonadisme en gevolglik impotensie as gevolg van hipotalamiese en / of pituïtêre onvoldoendeheid, wat lei tot 'n skending van die vrystelling van die hormoon gonadotropien. In gevalle van oortollige ystervoorrade vyf keer of meer, vind hiperpigmentasie van die vel plaas, wat die gevolg is van die afsetting van yster en melanien. Ysteroorlading van makrofage kan lei tot verswakte fagositose en verlaagde immuniteit, wat kan lei tot 'n verhoogde risiko van infeksie deur Listeria, Yersinia enterocolitica en Vibrio vulnificus. Afsetting van yster in die skildklier veroorsaak gewoonlik hipotireose.
Die ontwikkelde stadium van hemochromatose word gekenmerk deur die teenwoordigheid van sirrose, diabetes mellitus en velpigmentasie (die sogenaamde brons diabetes). By pasiënte wat alkohol misbruik en met hepatitis B en / of C besmet is, verloop die patologie van die lewer en pankreas wat met hemochromatose geassosieer word, 1-3 meer.
Die diagram toon diagnostiese maatreëls vir vermoedelike hemochromatose. Dit is bekend dat slegs ongeveer 70% van die C282Y-homosigote verhoogde vlakke van ferritien het, wat ooreenstem met 'n toename in ysterwinkels, en slegs 'n klein persentasie van hierdie pasiënte het kliniese manifestasies van die siekte. Natuurlik moet alle pasiënte met simptome wat met hemochromatose kan voorkom, verdere ondersoek ondergaan om die siekte uit te sluit. Daar moet veral aandag gegee word aan pasiënte met ongemotiveerde swakheid, artralgie, pyn in die regterkantste kwadrant van die buik, impotensie, verminderde libido, hartversaking-sindroom, velpigmentasie en diabetes. Daarbenewens is dit by alle pasiënte met hepatomegalie, sitolitiese sindroom, met die sirrotiese stadium van die siekte, benewens alle moontlike etiologiese oorsake van die siekte, die moontlikheid van hemochromatose nodig om te onthou. Natuurlik moet oorerflike hemochromatose uitgesluit word by pasiënte met familielede van die eerste verwantskap wat aan hemochromatose ly. 
Die studie moet begin deur die versadiging van serumtransferrin of serumferritienkonsentrasie te meet. Daar moet op gelet word dat die bepaling van transferrin in gevalle van eritropoëtiese hemochromatose nie so effektief is vir die verifiëring van die ysteroorlading sindroom nie. Die spesifisiteit van ferritien hang grootliks af van die teenwoordigheid van inflammatoriese siektes. As die vlak van ferritien hoër is as 200 μg / l by vroue of 300 μg / l by mans, of transferrinversadiging meer is as 40% by vroue of 50% by mans, is verdere toetsing nodig om hemochromatose 1, 2, 10, 11 uit te sluit.
Volgens die aanbevelings van die American Association for the Study of Liver Diseases 2011 (AASLD 2011) as die pasiënt 'n serumtransferrin van 1000 mg / l het, en afhangende van hierdie aanwysers, word 'n besluit geneem oor die terapeutiese taktiek en die behoefte aan 'n lewerbiopsie (sien grafiek ).
In pasiënte met 'n kombinasie van heterozygote C288Y / H63D, sowel as C288Y heterozygote of nie C288Y, is 'n noukeurige uitsluiting van ander siektes in die lewer of bloed nodig (indien nodig is 'n biopsie van die lewer nodig) en dan word 'n besluit geneem oor terapeutiese bloedvergieting.
Daar is geen betroubare bewyse dat sekere diëte die aanvang of vordering van hemochromatose beïnvloed nie. Sommige skrywers meen egter dat pasiënte met oorerflike hemochromatose 'n dieet getoon het, met die uitsondering van tee- en sitrusvrugte, wat volgens hulle bydra tot die ophoping van yster. Natuurlik moet alkohol, wat die belangrikste hepatotoksiese middel is, streng verbied word vir pasiënte met hemochromatose. Daar is ook bewys dat etanol hepcidiensintese 20, 21 verminder.
Die primêre behandeling vir primêre hemochromatose is bloedvergieting. Die vermindering van die aantal rooibloedselle, wat die belangrikste mobilisasie van yster in die liggaam is, en sodoende word die giftige effek van yster verminder en verminder. Pasiënte mag 50-100 bloedvlegsels per jaar, 500 ml elk, benodig om die ystervlakke na normaal te verlaag. Sodra die ystervlak genormaliseer is, is dit nodig om lewenslange, maar minder gereeld bloedvergieting te doen, gewoonlik 3-4 keer per jaar. Die doel van bloedvergieting is om ferritienvlakke van 50-100 ug / L te handhaaf. In die geval van 'n beduidende afname in hemoglobien na bloedvergieting, word gewrigsbehandeling met eritropoiëtien aanbeveel.
As hemochromatose opgemerk word in 'n vroeë stadium van die siekte, kan die behandeling van bloedverligting die funksionering van die betrokke organe voorkom en sodoende die lewensverwagting van die pasiënt verhoog. Pasiënte leef egter selde meer as twee jaar na diagnose, in gevalle van laat diagnose op die stadium van gedetailleerde kliniese manifestasies 22, 23.
Volgens die European Association for the Study of the Liver (EASL 2010) is aanduidings vir terapeutiese bloedverligting verhoogde vlakke van serumferritien. Daar word aanbeveel dat terapeutiese bloedvertering met 'n volume van 400-500 ml een keer per week of een keer elke 2 weke uitgevoer word totdat 'n ferritienvlak van 45% bereik is en 'n beduidende toename in serumferritien tot 1444 mcg / l, die diagnose van hemochromatose onmiskenbaar is. DNA-monsters is geanaliseer vir mutasies in die HFE-geen - 'n mutasie C282Y (c.845 G> A) is gevind in die homosigotiese toestand s.845A / s.845 A.
Die diagnose van pasiënt K. is dus oorerflike hemochromatose, 'n homosigotiese mutasie in die HFE-geen (C288Y / C288Y) met oorheersende lewerskade, graad 1 fibrose (FibroScan, Metavir 6,6 kPa).
Die laat manifestasie en diagnose van die siekte op die ouderdom van 58 in 2015 is te danke aan die langtermynvergoeding van die siekte as gevolg van massiewe bloedverlies as gevolg van menstruele bloed, bloedskenking, bloedverlies tydens beëindiging van swangerskap en bevalling.
Dit is opmerklik dat 8 jaar verloop het vanaf die voorkoms van die eerste tekens van die siekte tot die verifiëring van die diagnose! Sedert die einde van 2015 word die behandeling van die pasiënt voorgeskryf - bloedverhitting van 500 ml een keer per week. Die pasiënt het bloedvergieting goed verdra en het na die eerste prosedure 'n beduidende toestand in die toestand opgemerk. 'N Algemene bloedtoets en bloedferritien is gemonitor, waarvan die vlak geleidelik daal. In totaal is meer as 100 bloedvergieting in 2 jaar uitgevoer, maar tot dusver is die teiken oordragvlak (100 μg / l) nie bereik nie, omdat die pasiënt die prosedure periodiek oorgeslaan het, wat haar goeie gesondheid verklaar. Op die oomblik gaan die pasiënt voort met die terapie, en het daarin geslaag om haar te oortuig van die behoefte aan lewenslange terapie.
Daar moet dus onthou word dat in die teenwoordigheid van 'n sitolitiese sindroom by pasiënte, oorerflike hemochromatose by die diagnostiese soektog ingesluit moet word. Die terapie wat gekies word vir oorerflike hemochromatose bly tans bloedvergieting. Met voldoende terapie wat betyds begin is, word die ontwikkeling van die sirrotiese stadium van die siekte vermy en sodoende die lewensverwagting van pasiënte verhoog.
Inligting oor die outeurs:
Voloshina Natalya Borisovna - kandidaat vir mediese wetenskappe, medeprofessor propedeutiek van interne siektes van die mediese fakulteit
Osipenko Marina Fedorovna - dokter in mediese wetenskappe, prof., hoof. dept. propedeutiek van interne siektes van die mediese fakulteit
Voloshin Andrey Nikolaevich - Dokter van die Novosibirsk-kliniese hospitaal 2
Hemochromatose: wat is hierdie siekte?
Om die wese van die siekte te verstaan, moet u weet hoeveel yster normaalweg moet wees. By mans is yster ongeveer 500-1500 mg, en by vroue 300 tot 1000 mg. Die aanwysers hang nie net van geslag af nie, maar ook van die persoon se gewig. Meer as die helfte van die totale hoeveelheid yster is in hemoglobien.
Sowat 20 mg van hierdie mikro-element kom per dag met die voedsel in. Hiervan word slegs 1-1,5 mg in die ingewande opgeneem. Met hemochromatose (GC) of siderofilie, soos hierdie siekte ook genoem word, neem absorpsie toe tot 4 mg per dag, en word yster geleidelik in die weefsel van verskillende organe versamel.
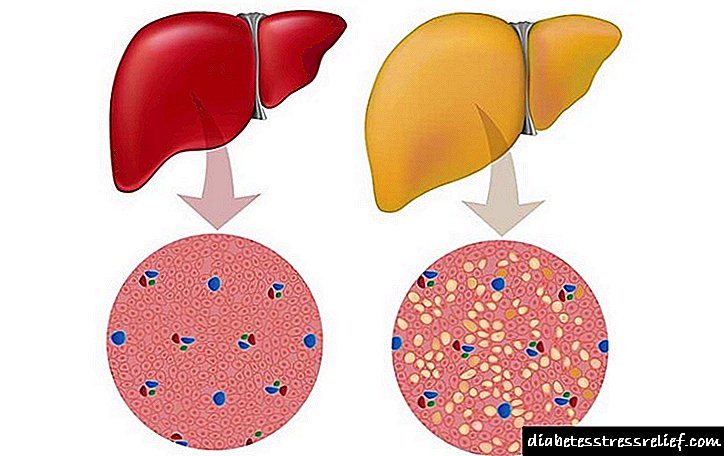
Gesonde lewer- en hemochromatose
Die oormaat daarvan vernietig die molekules van proteïene en koolhidrate, en dus ook die orgaan. By pasiënte met GC kan die hoeveelheid yster in die lewer 1% van die droë massa van die orgaan bereik, belaai met sirrose, en in 'n derde van die gevalle met lewerkanker. Beskadig deur oortollige yster, kan die pankreas die stimulus gee vir die ontwikkeling van suikersiekte.
As yster in die pituïtêre klier neergelê word, vernietig dit die hele endokriene stelsel. Voortplantingsorgane ly meer as ander: mans het erektiele disfunksie, en vroue kan onvrugbaarheid ontwikkel.
Oorsake van voorkoms
Die hoofrede vir GC is die 'wanfunksionering' van die geen, of eerder die HFE-geen. Dit is hy wat die verloop van chemiese prosesse en die hoeveelheid yster wat as deel van voedsel inkom, reguleer. Die mutasie wat daarin voorkom, lei tot ontwrigting van die ystermetabolisme.
Ander oorsake van GC is:
- talassemie. In hierdie geval word die hemoglobienstruktuur vernietig met die vrystelling van yster,
- hepatitis,
- yster kan toeneem as gevolg van gereelde bloedoortappings. Die feit is dat die leeftyd van uitheemse rooibloedselle baie korter is as hul eie. As hulle sterf, laat hulle yster los,
- hemodialise prosedures.
ICD-10-kode en klassifikasie
In die algemeen aanvaarde klassifiseerder van GC-siektes word kode E83.1 toegeken.
In 'n etilogiese aar word onderskei tussen primêre (of oorerflike GC) en sekondêr:
- primêre. Hierdie tipe siekte het 'n oorerflike aard en is die gevolg van 'n defek in die ensiemstelsel wat die ystermetabolisme beïnvloed. Dit word by drie mense uit 1000 gediagnoseer. Daar word opgemerk dat mans meer vatbaar is vir hierdie patologie en drie keer meer gereeld daaraan ly as vroue,
- sekondêre. Die oorsaak daarvan is die lewersiektes van die pasiënt (wat gereeld met alkoholisme waargeneem word), bloedoortapping, selfbehandeling met vitamienkomplekse met 'n hoë ysterinhoud. Die oorsaak van verworwe GC kan velprobleme en bloedsiektes wees.
Primêre hemochromatose (PCH) word gekenmerk deur 'n geleidelike ontwikkeling, en in die vroeë stadium kla die pasiënt van moegheid. Hulle kan gepla word deur pyn aan die regterkant en droë vel.
Die uitgebreide fase van PCH word gekenmerk deur:
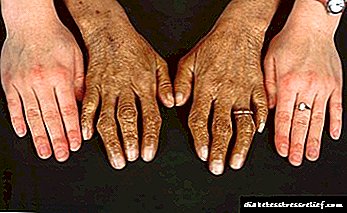
- spesifieke pigmentasie van die gesig, nek, arms en oksels. Hulle trek 'n brons kleur in,
- sirrose van die lewer. Dit word in 95% van die gevalle gediagnoseer,
- hartversaking
- artritis,
- diabetes mellitus: in 50% van die gevalle,
- vergrote milt,
- seksuele disfunksie.
In die laaste stadiums word portaal hipertensie en ascites waargeneem. Lewerkanker kan ontwikkel.
 Aangesien oortollige yster deur die jare gevorm word, word die aanvanklike simptome van sekondêre GC na 40 jaar by mans en by vroue na 60 jaar gemanifesteer.
Aangesien oortollige yster deur die jare gevorm word, word die aanvanklike simptome van sekondêre GC na 40 jaar by mans en by vroue na 60 jaar gemanifesteer.
Die simptome is soos volg:
- melasma,
- moegheid en gewigsverlies,
- verminderde libido
- vergroting en verdigting van lewerweefsel,
- sirrose (in die laaste stadium van GC).
Bloedtoets en ander diagnostiese metodes
 'N Gastro-enteroloog bevestig die diagnose. In die vroeë stadiums van die siekte is laboratoriumtoetse baie belangrik.
'N Gastro-enteroloog bevestig die diagnose. In die vroeë stadiums van die siekte is laboratoriumtoetse baie belangrik.
Met GC word spesiale bloedtoetse uitgevoer om die waardes van yster in die plasma, die lae ysterbindingsvermoë daarvan en versadiging met transferrien op te spoor.
Die belangrikste simptoom van die siekte is hemosiderienafsettings in die hepatosiete van die lewer, in die vel en ander organe, wat 'roes' word as gevolg van die oorskot van hierdie pigment. 'N Algemene bloedtoets is ook nodig vir biochemie, sowel as suiker. Daarbenewens word lewertoetse gedoen.
 Daarbenewens word instrumentele studies ook uitgevoer:
Daarbenewens word instrumentele studies ook uitgevoer:
- lewerbiopsie is die belangrikste manier om GC te bevestig,
- Ultraklank van die buik
- Lewer MRI (in sommige gevalle)
- echokardiografie, om kardiomyopatie uit te sluit / te bevestig,
- gesamentlike radiografie.
Terapeutiese dieet
Dit is belangrik om te verstaan dat die dieet lewenslank moet wees met 'n gediagnoseerde hemochromatose.
Die belangrikste reël is die maksimum vermindering in die dieet van produkte wat yster bevat, veral:

- harde kaas en seevis,
- graan: hawer, gierst en bokwiet,
- swart brood
- peulgewasse en droëvrugte,
- askorbiensuur en medisyne met 'n hoë inhoud van vitamien C,
- afval, veral die lewer, is heeltemal uitgesluit.
Alkohol is 'n absolute taboe. Inteendeel, maar tee en koffie word gewys. Hulle het tannien, wat die opname van yster vertraag.
Lys van medisyne wat gebruik is
Hierdie behandeling word uitgevoer met medisyne wat yster uit die liggaam van die pasiënt verwyder. In die beginfase word vitamiene A, E en foliensuur voorgeskryf. Dan word chelators (soos Desferal) gebruik.

Inspuiting dosis: 1 g / dag. Reeds 500 mg van die middel gee 'n tasbare resultaat: tot 43 mg yster word uitgeskei. Die kursus duur tot 1,5 maande. Langdurige gebruik is gevaarlik: lensvergroeiing is moontlik.
Flebotomie en ander terapeutiese prosedures
 Flebotomie is die eenvoudigste en terselfdertyd redelik effektiewe nie-farmakologiese behandeling van GC.
Flebotomie is die eenvoudigste en terselfdertyd redelik effektiewe nie-farmakologiese behandeling van GC.
Daar word 'n gat in die pasiënt se bloed gemaak, en bloed word uit die liggaam vrygestel. Ongeveer 500 ml word per week gedreineer.
Die prosedure is slegs buitepasiënt. Bloed word voortdurend getoets vir ferrienkonsentrasie: dit moet daal tot 50. Dit kan 2-3 jaar duur. Die terapie is verder daarop gemik om die optimale waarde van hierdie spoorelement te handhaaf.
Behandeling met volksmiddels
Hierdie terapie het 'n ligte effek op organe wat siek is.
Lewer behandeling:

- pampoen. Dit is goed sowel as gebak. Groente word by slaaie gevoeg of met heuning gemeng - lekker en gesond! Daar word ook pampoensap gewys: 'n halwe glas op 'n leë maag,
- beet- Nog 'n nuttige produk vir GC. Gebruik dit in rou of gekookte vorm. Gesonde en vars pers sap.
Vir hartbehandeling kan u infusies van meidoorn, adonis of moederwortel aanbeveel. Kruie word met kookwater gegiet en word dringend volgens die instruksies gedrink.
Pankreasbehandeling:

- plantaad-afkooksel sal help. Proporsies: 1 eetlepel. grondstowwe tot 1 eetlepel. water. Gebraaide sade word vir 5 minute gekook, afgekoel en voor etes geneem, 1 eetlepel.,
- heuning met kaneel. Proporsies: 1 eetlepel. poeier tot 1 eetlepel water. Dring aan op 15-30 minute. en voeg heuning by. Laat staan vir nog 2 uur. Alle middele moet binne 'n dag gedrink word.
Nuttige en ongekookte hawermeel (met skil). Gedeeltes: 100 g graan tot 1,5 liter water. Kook vir minstens 'n halfuur. Dan, reg in die bak waar die hawer gekook is, fyngemaak tot fyngemaak en kook weer vir 40 minute. Die lewensduur van die gefiltreerde sous is nie langer as twee dae nie. Drink 'n halwe glas voor etes.
Prognose en hoof kliniese riglyne
Maar as die terapie onder mediese toesig en betyds uitgevoer word, neem die pasiënt se lewe aansienlik toe.
Aangesien dit 'n oorerflike siekte is, word hemochromatose in 25% van die gevalle by die pasiënt se familielede gediagnoseer. Hulle moet dus verder ondersoek word. Dit sal die siekte onthul selfs voor kliniese manifestasies en in die toekoms om die komplikasies daarvan te vermy.
In die geval van sekondêre GC word dieet aanbeveel, dit is belangrik om die toestand van die lewer en bloed onder beheer te hou. Hemochromatose wat tydens swangerskap (of tydens die beplanningstadium) opgespoor word, is nie gevaarlik nie.
Verwante video's
Oor die simptome, oorsake en behandelingsmetodes vir hemochromatose in die video:
Ongelukkig is die oorsaak van hemochromatose nog nie geïdentifiseer nie. Maar tans word 'n spesiale omvattende behandelingstegniek ontwikkel en aktief gebruik, met die doel om die kliniese manifestasies van die siekte te onderbreek en die risiko van moontlike komplikasies te verminder.
- Stabiliseer die suikervlakke vir 'n lang tyd
- Herstel pankreas insulienproduksie
Kom meer te wete. Nie 'n dwelm nie. ->
Gelyktydige siekteterapie
Oormatige yster in organe lei tot die ontwikkeling van veelvuldige patologieë. Almal benodig aanvullende terapie. As GC byvoorbeeld bygedra het tot die ontwikkeling van suikersiekte, moet laasgenoemde behandel word, en die suiker dosis onder beheer moet bly.
As patologieë in die lewer opgespoor word, duur die behandeling voort. Dit is nodig om die ontwikkeling van patologie tot 'n kwaadaardige gewas te voorkom.
Hemochromatose
Erflike hemochromatose (NG) is 'n polisistemiese siekte wat gebaseer is op geneties bepaalde metaboliese afwykings van yster, wat lei tot die oormatige ophoping daarvan in die liggaam en toksiese skade aan organe en weefsel.
Die eerste beskrywing van die siekte behoort aan A. Trousseau (1865), wat 'n drieling van die belangrikste kliniese manifestasies geïdentifiseer het: diabetes mellitus, bronsvelpigmentasie, sirrose. Die term "hemochromatosis" is in 1889 deur F.D. von Recklinghausen. Sedert 1935 behoort die siekte aan die groep oorerflike siektes. In 1996 het J.N. Feder et al. die geen vir oorerflike hemochromatose (HFE) geïdentifiseer, waarvan mutasies meestal tot die ontwikkeling van hierdie siekte lei. In 2000-2004 mutasies van ander gene wat tot die ontwikkeling van hemochromatose lei, word beskryf.
Die voorkoms van die siekte wissel van 1: 250 individue wat in Noord-Europa woon tot 1: 3300 onder die swart bevolking van die VSA en Afrikalande. Die siekte word 5-10 keer meer gereeld by mans gediagnoseer as by vroue. Tydens genetiese sifting is daar gevind dat 'n homosigotiese mutasie van die HFE-geen by 1 uit 500 ondersoeke pasiënte opgespoor word, terwyl die aantal klinies gevestigde gevalle van NG 1: 5000 is. Dus word 'n beduidende aantal gevalle nie laat erken of gediagnoseer nie, in die stadium van onomkeerbare interne skade. organe (sirrose, diabetes mellitus, verwaterde kardiomiopatie).
In ooreenstemming met die genetiese basis van die siekte word 4 soorte oorerflike hemochromatose onderskei:
Tipe I - geërf deur 'n outosomale resessiewe meganisme, as gevolg van mutasies in die HFE-geen op chromosoom 6. Die C282Y-mutasie word meestal (by 87-90% van die pasiënte) aangeteken - die vervanging van cysteïne deur tyrosien in die 282ste aminosuur. Die H63D-mutasie kom minder voor - die vervanging van sitidien met guanien in die 63ste aminosuur,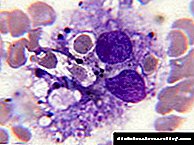
Tipe II - jeugdhemochromatose is skaars, weens mutasies in die geen wat verantwoordelik is vir die sintese van 'n ander proteïen van ystermetabolisme - hepsidien,
Tipe III - die genetiese basis bestaan uit mutasies van 'n geen wat codeer vir die sintese van transferrienreseptore,
Tipe IV - die genetiese basis bestaan uit mutasies in die SLC40A1-geen, wat die sintese van die vervoerproteïne ferroportien kodeer.
Etiologie en patogenese
Yster is enersyds 'n noodsaaklike biochemiese komponent van die belangrikste metaboliese prosesse en is 'n potensieel giftige element wat oksidatiewe skade aan biologiese membrane, proteïene en nukleïensure kan veroorsaak. In ooreenstemming hiermee word ysterhostostase in die menslike liggaam streng gereguleer. Die meeste van hierdie elemente ondergaan 'n herwinningsproses: makrofage van die milt en lewer vang en vernietig verouderde rooibloedselle, voer die agteruitgang van hemoglobien uit en die vrylating van yster, wat bind aan transferrin of ferritien en word herwin. Die daaglikse fisiologiese verlies aan yster is nie meer as 1-2 mg nie en word gekompenseer deur die opname van 'n ekwivalente hoeveelheid yster in die spysverteringskanaal. Daar is geen meganismes wat die eliminasie van yster by mense beheer nie.
Mutasies in die gene wat verantwoordelik is vir die sintese van proteïene wat by ystermetabolisme betrokke is, lei tot 'n wanbalans tussen die inname en verlies van yster, die patologiese opeenhoping van hierdie element in organe en weefsel, en die voorkoms van vry (nie geassosieer met transferrin) yster in die bloed. Die ontwikkeling van tipe I-hemochromatose hou verband met 'n mutasie van die geen wat verantwoordelik is vir die sintese van die HFE-proteïen (hemochromatosis-proteïen), wat 'n glikoproteïen is (MM = 37.235 dalton), soortgelyk aan struktuur as die proteïene van die belangrikste histokompatibiliteitskompleks van klas 1. Die funksie van die HFE-proteïen in ystermetabolisme en die meganisme van die skerp toename in ysterabsorpsie tydens mutasies in die HFE-geen is nog nie volledig vasgestel nie.
Die patogenese van tipe II-IV hemochromatose word geassosieer met mutasies van gene wat kodeer vir ander proteïene wat betrokke is by ystermetabolisme - hepsidien, transferrinreseptor-II, ferroportien.
'N Kenmerkende kenmerk van tipe IV NG, wat gebaseer is op mutasies van die ferroportiengeen, is 'n oorheersende oortreding van ysterherwinningsprosesse, wat fenotipies manifesteer as diep hipochromiese anemie en eritropoïese van ystertekort in kombinasie met ernstige hemochromatose van interne organe.
Die patologiese opeenhoping van yster in die parenchymale organe hou verband met degeneratiewe veranderinge in die sellulêre parenchiem en die progressiewe ontwikkeling van veselagtige weefsel, wat lei tot onomkeerbare disfunksie van vitale organe. Die lewer-, hart- en pankreas is die kwesbaarste teikenorgane.
Kliniese tekens en simptome
Die kliniese beeld van NG word bepaal deur die ophopingsvlak van yster in organe en weefsels. Met tipe I-hipertensie word kliniese manifestasies gewoonlik aangetref op die ouderdom van 45-50 jaar en ouer. By jong hemochromatose (tipe II) verskyn ernstige lewer- en hartletsels vroeg - in die tweede of derde dekade van die lewe. By mans word die kliniese manifestasies van die siekte 3 keer meer gereeld waargeneem as by vroue, wat verband hou met die fisiologiese eienskappe van die vroulike liggaam. Die belangrikste kliniese manifestasies sluit in simptome van skade aan die lewer, hart, organe van die endokriene stelsel en gewrigte.
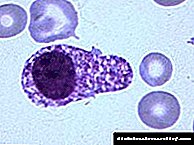 Tekens van lewerskade kan tydens 'n ewekansige ondersoek opgespoor word in die vorm van 'n ongemotiveerde toename in transaminases of debuut met simptome van portaal hipertensie: ascites, hepatosplenomegaly, bloeding van spatare van die slukderm en maag.
Tekens van lewerskade kan tydens 'n ewekansige ondersoek opgespoor word in die vorm van 'n ongemotiveerde toename in transaminases of debuut met simptome van portaal hipertensie: ascites, hepatosplenomegaly, bloeding van spatare van die slukderm en maag.
Simptome van hartskade is hartaanvalle, die ontwikkeling van aritmieë en tekens van hartversaking. Erge kardiomyopatie is die grootste oorsaak van dood by jong pasiënte.
Die ontwikkeling van diabetes en disfunksie van geslagskliere is kenmerkende simptome van NG. By mans word testikulêre atrofie, verminderde seksdrang, impotensie, azoospermie gereeld by vroue waargeneem - amenorree, onvrugbaarheid.
Skade aan die gewrigte word gemanifesteer deur aanhoudende artralgie, die metakarpophalangeale gewrigte is meestal betrokke, minder gereeld die knie-, heup- en elmbooggewrigte. Die styfheid van die gewrigte ontwikkel geleidelik.
Ander kliniese manifestasies van NG sluit in duidelike ongemotiveerde swakheid, moegheid, slaperigheid, buikpyn van verskillende intensiteit en lokalisering, hiperpigmentasie van die vel, en 'n neiging tot verskillende infeksies (insluitend mikroörganismes wat selde gesonde mense beïnvloed - Yersenia enterocolitica en Vibrio vulnificus).
Die diagnose van NG word bepaal op grond van 'n kenmerkende kliniese en laboratoriumbeeld.Dit is maklik om die diagnose van hemochromatose by 'n pasiënt te vermoed met 'n kombinasie van die volgende simptome: artralgie, buikpyn, bronsgrys vel, die teenwoordigheid van diabetes mellitus en hepatomegalie.
Bloedtoets: 'n kombinasie van 'n hoë hemoglobienvlak met 'n lae hemoglobienkonsentrasie in eritrosiete (MCH) is kenmerkend. Die ontwikkeling van bloedarmoede of ander sitopenie word in die laat stadiums van die siekte waargeneem - by pasiënte met sirrose van die lewer, of as gevolg van talle bloedvergieting.
Studie van ystermetabolisme wat nodig is om laboratoriumtekens van ysteroorlading te identifiseer en omvat die bepaling van die vlak van yster, ferritien en transferrin van bloedserum, totale ysterbindingsvermoë van serum (OZHSS) en die geskatte transferrinversadigingskoëffisiënt van yster (NTZH). NG word gekenmerk deur 'n toename in serumyster- en ferritienvlakke, 'n afname in die vlakke van OGSS en transferrin. 'N Belangrike laboratoriumteken van hemochromatose is 'n toename in die SOI-koëffisiënt by mans bo 60%, by vroue - bo 50%.
Uitsteltoets bevestig die teenwoordigheid van ysteroorlading: na binnespierse 0,5 g deferoksamien (desferaal), is die daaglikse uitskeiding van yster in urine aansienlik hoër as die normale vlak (0-5 mmol / dag).
In tipe IV NG kan die laboratoriumbeeld voorgestel word deur diep hipochromiese anemie, hiposiderinemie en verhoogde serumferritien, wat gekombineer word met ernstige oorlading van weefsel met yster.
Molekulêre genetiese analise uitgevoer laat u toe om die oorerflike aard van hemochromatose te bevestig en die sekondêre aard van ysteroorlading uit te sluit. Die diagnose van NG word bepaal in die teenwoordigheid van homosigotiese mutasies van die HFE-geen (C282Y of H63D) of wanneer komplekse heterozygote ('n kombinasie van heterosigotiese mutasies C282Y en H63D) opgespoor word by pasiënte met laboratoriumtekens van ysteroorlading. Geïsoleerde, heterosigotiese mutasies C282Y en H63D word aangetref in die bevolking van gesonde mense met 'n frekwensie van onderskeidelik 10,6% en 23,4%, en die teenwoordigheid van hierdie mutasies is nie die basis vir die diagnose van NG nie.
CT-skandering van abdominale organe onthul 'n verhoogde digtheid van lewerweefsel as gevolg van ysterafsettings en laat die teenwoordigheid van hemochromatose vermoed word.
Met MRI die lewer van 'n pasiënt met hemochromatose het 'n donkergrys of swart kleur. CT en MRI van die lewer is nodig om die diagnose van hepatosellulêre karsinoom uit te sluit.
Lewerbiopsie Met 'n semi-kwantitatiewe of kwantitatiewe bepaling van die ysterinhoud kan u die mate van ontwikkeling van fibrose en die konsentrasie van yster in die lewerweefsel bepaal. Vir die diagnose van hemochromatose word aanbeveel om die 'lewer-ysterindeks' te bereken, wat gelyk is aan die verhouding van die ysterinhoud in die lewerweefsel (in mikromol / g droë gewig) tot die ouderdom van die pasiënt (in jare). 'N Indeks> 2.0 bevestig die diagnose van NG.
Erflike hemochromatose moet onderskei word met sekondêre ysteroorlading-sindrome wat ontwikkel by pasiënte met oorerflike en verworwe hemolitiese anemie, sommige vorme van myelodysplastiese sindroom (refraktiewe sideroblastiese anemie), porfirie, sowel as by pasiënte met alkoholiese lewerskade.
Die doel van die behandeling van NG is om oortollige yster uit die liggaam te verwyder en onomkeerbare skade aan interne organe te voorkom. 'N Algemene behandelingsmetode is bloedvergieting. Die aanvanklike kursus bestaan uit bloedvergieting in 'n volume van 500 ml een keer per week. Nadat die hemoglobienvlak met 15-20 g / l verlaag is, is die MCV-vlak met 3-5 fl. en die inhoud van serumferritien tot 20-50 ng / ml, gaan na onderhoudsterapie - verwydering van 500 ml bloed elke 2-4 maande by mans en elke 3-6 maande by vroue. Die behandeling is lewenslank.
In die teenwoordigheid van bloedarmoede of ander kontraindikasies (byvoorbeeld hartversaking) word ysterchelators gebruik vir bloedvergieting. Deferoxamine bind oortollige yster in weefsels en bloedserum en skei uit met uriene en ontlasting. Die geneesmiddel se halfleeftyd is egter kort - slegs 10 minute, wat stadig toediening verg: binneaars in die vorm van 3-4 uur infusies of onderhuids, verkieslik in die vorm van 12-uur- of 24-uur-infusies met spesiale pompe. Nuwe kompleksvormende middels vir orale toediening is ontwikkel en is in die stadium van kliniese studie of implementering, waarvan die effektiefste Deferasirox is.
Die effektiwiteit van behandeling word bepaal deur die dinamika van kliniese en laboratoriumdata. Die toestand van pasiënte begin na 'n verloop van bloedverligting verbeter: swakheid, moegheid, slaperigheid verdwyn, die grootte van die lewer neem af, die verloop van diabetes en kardiomiopatie kan verbeter. Laboratoriumkontrole sluit in die studie van hemogram, indikators van ferritien, yster en NTZH (1 keer in 3 maande), die vlak van urinaire uitskeiding.
In die geval van 'n vroeë diagnose van hipertensie en tydige terapeutiese bloedverligting, is die prognose gunstig: pasiënte se lewensverwagting verskil nie van die lewensverwagting van mense wat nie aan hemochromatose ly nie. In die geval van laat diagnose van die siekte, in die teenwoordigheid van lewersirrose, kardiomiopatie, diabetes mellitus, word die prognose bepaal deur die erns van hierdie onomkeerbare komplikasies. Die belangrikste oorsake van die dood van pasiënte is: komplikasies van suikersiekte, hartversaking, primêre lewerkanker, lewerversaking, bloeding van spatare van die slukderm en maag, tussenstroom infeksies.
Algemene inligting
Hemochromatosis (brons diabetes, pigmentêre sirrose) is 'n genetiese oorsaak van 'n skending van ystermetabolisme, wat lei tot die afsetting van ysterbevattende pigmente in weefsel en organe en die ontwikkeling van veelvuldige orgaanversaking. Die siekte, gepaard met 'n kenmerkende simptoomkompleks (velpigmentasie, lewersirrose en diabetes mellitus), is in 1871 beskryf, en in 1889 word dit hemochromatose genoem vir die kenmerkende kleur van die vel en interne organe. Die frekwensie van oorerflike hemochromatose in 'n populasie is 1,5-3 gevalle per 1000 bevolking. Mans ly 2-3 keer meer gereeld aan hemochromatose as vroue. Die gemiddelde ouderdom van die ontwikkeling van patologie is 40-60 jaar. Vanweë die polisistemiese aard van die letsel, is verskillende kliniese dissiplines betrokke by die studie van hemochromatose: gastro-enterologie, kardiologie, endokrinologie, rumatiek, ens.
In die etiologiese aspek word primêre (oorerflike) en sekondêre hemochromatose onderskei. Primêre hemochromatose word geassosieer met 'n defek in ensiemstelsels, wat lei tot die afsetting van yster in die interne organe. Afhangend van die geenafwyking en die kliniese beeld, word 4 vorme van oorerflike hemochromatose onderskei:
- I - klassieke outosomale resessiewe, HFE-geassosieerde tipe (meer as 95% van die gevalle)
- II - jeugdige tipe
- III - oorerflike HFE-ongeassosieerde tipe (mutasies in die transferrienreseptor tipe 2)
- IV– outosomale dominante tipe.
Sekondêre hemochromatose (veralgemeende hemosiderose) ontwikkel as gevolg van die verwerkte onvoldoendeheid van ensiemstelsels wat by ystermetabolisme betrokke is, en word dikwels geassosieer met ander siektes, in verband met die onderskeie variante daarvan: post-transfusie, voeding, metabolisme, gemeng en neonataal.
In die kliniese verloop gaan hemochromatose deur drie fases: I - sonder ysteroorlading, II - met ysteroorlading, maar sonder kliniese simptome, III - met die ontwikkeling van kliniese manifestasies.

Oorsake van hemochromatose
Primêre oorerflike hemochromatose is 'n outosomale resessiewe oordragsiekte. Dit is gebaseer op mutasies van die HFE-geen op die kortarm van die 6de chromosoom. 'N Defek in die HFE-geen lei tot die ontwrigting van die transferrin-bemiddelde opname van yster deur die selle van die duodenum 12, wat lei tot die vorming van 'n valse sein oor ystertekort in die liggaam. Op sy beurt dra dit by tot die verhoogde sintese van die ysterbindende proteïen DCT-1 deur enterosiete en die verhoogde opname van yster in die ingewande (met die normale inname van spoorelemente uit voedsel). In die toekoms is daar 'n buitensporige afsetting van die ysterbevattende hemosiderienpigment in baie interne organe, die dood van hul funksioneel aktiewe elemente met die ontwikkeling van sklerotiese prosesse. Met hemochromatose word jaarliks 0,5-1,0 g yster in die menslike liggaam opgehoop, en die manifestasies van die siekte manifesteer wanneer die totale ystervlak van 20 g bereik word (soms 40-50 g of meer).
Sekondêre hemochromatose ontwikkel as gevolg van die oormatige eksogene inname van yster in die liggaam. Hierdie toestand kan voorkom by gereelde herhaalde bloedoortappings, onbeheerde inname van ysterpreparate, thalassemie, sommige soorte bloedarmoede, velporfyrië, alkoholiese sirrose van die lewer, chroniese virale hepatitis B en C, kwaadaardige neoplasmas, na 'n dieet met 'n lae proteïen.
Simptome van hemochromatose
Die kliniese manifestasie van oorerflike hemochromatose kom voor in volwassenheid, wanneer die totale ysterinhoud in die liggaam kritieke waardes bereik (20-40 g). Afhangend van die heersende sindrome, word hepatopatiese (lewerhemochromatose), kardiopatiese (harthemochromatose) onderskei, endokrinologiese vorme van die siekte.
Die siekte ontwikkel geleidelik, in die beginfase oorheers nie-spesifieke klagtes oor verhoogde moegheid, swakheid, gewigsverlies, verminderde libido. Op hierdie stadium kan pasiënte deur die pyn in die regte hipochondrium, droë vel, artralgie versteur word as gevolg van chondrocalcinosis van groot gewrigte. In die uitgebreide stadium van hemochromatose word 'n klassieke simptoomkompleks gevorm, voorgestel deur velpigmentasie (bronsvel), sirrose, diabetes mellitus, kardiomyopatie, hipogonadisme.
Die vroegste teken van hemochromatose is gewoonlik die voorkoms van 'n spesifieke kleur van die vel en slymvliese, veral uitgedruk op die gesig, nek, boonste ledemate, in die oksels en geslagsdele en vel. Die intensiteit van pigmentasie hang af van die duur van die siekteverloop en wissel van liggrys (rokerig) tot bronsbruin. Kenmerkend is haarverlies op die kop en stam, konkawe (lepelvormige) vervorming van die naels. Daar word kennis geneem van artrropaties van die metacarpophalangeale, soms knie-, heup- en elmbooggewrigte met die daaropvolgende ontwikkeling van hul styfheid.
By byna alle pasiënte word 'n toename in die lewer, miltmurgie en sirrose van die lewer waargeneem. Disfunksie van die pankreas kom tot uitdrukking in die ontwikkeling van insulienafhanklike diabetes mellitus. As gevolg van skade aan die pituïtêre klier tydens hemochromatose ly seksuele funksie: by mans ontwikkel testikulêre atrofie, impotensie, ginekomastie by vroue - amenorree en onvrugbaarheid. Harthemochromatose word gekenmerk deur kardiomyopatie en die komplikasies daarvan - aritmie, chroniese hartversaking, miokardiale infarksie.
In die terminale stadium van hemochromatose ontwikkel portaal hipertensie, ascites, kacheksie. Die dood van pasiënte vind gewoonlik as gevolg van bloeding van spatare van die slukderm, lewerversaking, akute hartversaking, diabetiese koma, aseptiese peritonitis, sepsis. Hemochromatose verhoog die risiko van lewerkanker (hepatosellulêre karsinoom) aansienlik.
Diagnose van hemochromatose
Afhangend van die heersende simptome, kan pasiënte met hemochromatose hulp soek by verskillende spesialiste: 'n gastroënteroloog, kardioloog, endokrinoloog, ginekoloog, uroloog, rumatoloog en dermatoloog. Intussen is die diagnose van die siekte dieselfde vir verskillende kliniese variante van hemochromatose. Na evaluering van die kliniese tekens word aan pasiënte 'n stel laboratorium- en instrumentele studies toegeken om die geldigheid van die diagnose te verifieer.
Laboratoriumkriteria vir hemochromatose is 'n beduidende toename in die vlak van yster, ferritien en transferrin in bloedserum, 'n toename in die uitskeiding van yster in urine, en 'n afname in die totale ysterbindingsvermoë van bloedserum. Die diagnose word bevestig deur die biopsie van die lewer of vel, in die monsters waarvan die hemosiderienneerslag opgespoor word. Die oorerflike aard van hemochromatose word bepaal as gevolg van molekulêre genetiese diagnostiek.
Ten einde die erns van die skade aan interne organe en die voorspelling van die siekte te bepaal, word lewertoetse, bloed- en urienglukosevlakke, glikosileerde hemoglobien, ens. Bestudeer. Laboratoriumdiagnose van hemochromatose word aangevul deur instrumentele studies: gewrigstradiografie, EKG, echokardiografie, ultraklank van die buikholte, MRI van die lewer, ens.
Hemochromatose behandeling
Die hoofdoel van die terapie is om oortollige yster uit die liggaam te verwyder en die ontwikkeling van komplikasies te voorkom. Aan pasiënte met hemochromatose word 'n dieet voorgeskryf wat voedsel wat hoog in yster is beperk (appels, vleis, lewer, bokwiet, spinasie, ens.), Maklik verteerbare koolhidrate. Dit is verbode om multivitamiene, askorbiensuur, voedingsaanvullings wat yster, alkohol bevat, te neem. Om oortollige yster uit die liggaam te verwyder, gebruik hulle bloedvergieting onder die beheer van hemoglobien, hematokrit en ferritien. Vir hierdie doel kan buitekorporale hemokorreksie metodes gebruik word - plasmaferese, hemosorpsie, sitaferese.
Patogenetiese geneesmiddelterapie van hemochromatose is gebaseer op intramuskulêre of intraveneuse toediening van deferoksamienbindende Fe3 + -ione aan 'n pasiënt. Terselfdertyd word simptomatiese behandeling van sirrose van die lewer, hartversaking, diabetes mellitus en hipogonadisme uitgevoer. By ernstige arthropatie word indikasies vir artroplastie (endoprotetika van aangetaste gewrigte) bepaal. By pasiënte met sirrose word die kwessie van leweroorplanting aangespreek.
Voorspelling en voorkoming van hemochromatose
Ondanks die progressiewe verloop van die siekte, kan tydige terapie die lewensduur van pasiënte met hemochromatose met etlike dekades verleng. In die afwesigheid van behandeling, is die gemiddelde lewensverwagting van pasiënte na diagnose van patologie nie meer as 4-5 jaar nie. Die teenwoordigheid van komplikasies van hemochromatose (hoofsaaklik lewersirrose en kongestiewe hartversaking) is 'n prognosties ongunstige teken.
Met oorerflike hemochromatose kom voorkoming op gesinsifting, vroeë opsporing en behandeling van die siekte. Rasionele voeding, monitering en toediening van ysterpreparate, bloedoortappings, weiering om alkohol te neem en monitering van pasiënte met siektes in die lewer- en bloedstelsel kan help om die ontwikkeling van sekondêre hemochromatose te voorkom.