Diabetes mellitus verslag
In die artikel word die gebruiksaanwysings, prys en analoë van Sitagliptin bespreek.
Dit word as fosfaatmonohydraat vervaardig. Die vrystelling daarvan is filmbedekte tablette.
Die geneesmiddel het beduidende verskille in farmakologiese werking en chemiese struktuur van analoë, sowel as afgeleides van alfa-glikosidase-remmers, biguaniede en sulfonylureas.

Inhibisie van DPP 4 deur middel van "Sitagliptin" veroorsaak 'n toename in die konsentrasie van die hormone HIP en GLP-1. Hierdie hormone is onder inkretiene. Hul afskeiding word in die ingewande gemaak.
As gevolg van eet neem die konsentrasie van sulke hormone toe. Die inkretiene vorm deel van die fisiologiese stelsel wat suikerhomeostase in die menslike liggaam reguleer. Analooges van Sitagliptin moet deur 'n dokter gekies word.
Kenmerke van farmakokinetika
Die middel word teen 'n hoë dosis opgeneem nadat dit deur die pasiënt gebruik is. Hierdie instrument het 'n perfekte biobeskikbaarheid van 87%. Die inname van vetterige voedsel beïnvloed nie die farmakologiese kinetika van die middel nie.
Die middel word onveranderd as 'n deel van die urine uitgeskei. Nadat die ontvangs gestaak is, word dit binne 'n week in die urine (87%) en ontlasting (13%) uitgeskei.
Dit word bevestig deur die gebruiksaanwysings met Sitagliptin. Analoge van die middel is vir baie van belang.
Indikasies vir die gebruik van die middel
Die middel word gebruik in die implementering van monoterapie as die pasiënt gediagnoseer is met tipe 2-diabetes mellitus. Hierdie middel word goedgekeur vir gebruik, ongeag voedselinname. Die kombinasie van Sitagliptin en Metformin kan as 'n komplekse behandeling in die teenwoordigheid van tipe II diabetes mellitus gebruik word.

In samewerking met Metformin is die aanbevole dosis 100 mg een keer per dag.
As u die tyd van toediening misloop, moet u Sitagliptin so gou as moontlik drink. Dit is te wyte aan die feit dat die gebruik van 'n dubbele dosis van die middel nie toegelaat word nie.
Dit is verbode om 'n middel gereeld te drink as wat in die instruksies aanbeveel word.
Die middel maak dit moontlik om suikers in die liggaam te beheer, maar hierdie middel behandel nie diabetes nie.
Die gebruik van die medisyne moet uitgevoer word as dit goed gaan met die pasiënt, stop die behandeling slegs na die aanbeveling en konsultasie van die behandelende geneesheer.
Het Sitagliptin enige analoë? Hieroor hieronder.
Instruksies vir die gebruik van die middel
"Sitagliptin" is 'n medisyne wat redelik goed verdra word as dit deur 'n pasiënt geneem word, nie net as monoterapie nie, maar as deel van 'n uitgebreide behandeling met ander middels met hipoglisemiese eienskappe.
Die belangrikste dosis van die middel word deur die niere uitgeskei. Hierdie metode om die aktiewe bestanddeel uit die menslike liggaam te verwyder, vereis dat 'n spesialis die gesondheid van hierdie liggaam moet monitor as die pasiënt nierversaking gehad het voordat hy die middel gebruik. Indien nodig, word die dosis wat geneem word, aangepas. As daar 'n ligte vorm van nierversaking is, word die dosisaanpassing van die middel nie uitgevoer nie.
As 'n pasiënt matige nierversaking het, moet die dosis van die medikasie nie meer as 50 mg per dag wees nie.Die middel kan te eniger tyd gebruik word, ongeag die prosedure, soos dialise.
As hierdie middel gebruik word as deel van 'n komplekse behandeling, moet die hoeveelheid sulfonielureumderivate wat geneem moet word verminder word om te voorkom dat sulfon-geïnduseerde hipoglisemie in die liggaam van die pasiënt voorkom.

Die dosering van die medisyne wat gebruik word, word deur die behandelende geneesheer bepaal sodra 'n volledige ondersoek gedoen word na die liggaam van die pasiënt wat aan die tweede tipe diabetes ly.
As daar 'n vermoede bestaan dat die ontwikkeling van pankreatitis in die liggaam van die pasiënt voorkom, is dit noodsaaklik om die gebruik van Sitagliptin en ander medisyne te stop wat moontlik die patologie kan vererger.
Voordat die middel gebruik word, moet 'n spesialis die pasiënt inlig oor die eerste spesifieke tekens van pankreatitis.
Dit word dus gesê in die gebruiksaanwysings vir "Sitagliptin." Pryse, resensies en analoë word hieronder aangebied.
Kontra
Die gebruik van hierdie middel kan 'n lewensgevaarlike, ernstige ontsteking van die pankreas in die menslike liggaam veroorsaak.
As die medisyne nie korrek gebruik word nie, kan dit baie newe-effekte in die liggaam veroorsaak. As die eerste simptome van oortredings voorkom, moet u onmiddellik 'n spesialis raadpleeg.
Gebruik die dwelmmiddel in ooreenstemming met die instruksies en in die korrekte hoeveelheid voorgeskryf deur die behandelende geneesheer.
As 'n middel gebruik word, moet daar in ag geneem word dat daar 'n hele reeks verskillende kontraindikasies is:
- die teenwoordigheid van die eerste tipe diabetes,
- hipersensitiwiteit,
- babatyd,
- diabetiese ketoasidose,
- borsvoeding
- die ouderdom van die pasiënt is minder as agtien jaar.
Pryse en analoë word nie in die gebruiksaanwysings met Sitagliptin aangedui nie.

Uitvoerbare newe-effekte
Tydens die gebruik van die middel by mense kan 'n hele paar newe-effekte voorkom. Van hulle word opgemerk:
- angioedema,
- jeuk,
- anafilakse,
- ledemaatpyn
- uitslag,
- rugpyn
- vel vaskulitis
- artralgie,
- urtikarie,
- mialgie,
- eksfoliatiewe velsiektes, Stevens-Johnson-sindroom,
- hoofpyn,
- akute pankreatitis,
- verswakte nieraktiwiteit, ontoereikendheid van hierdie orgaan in akute vorm, wat dialise benodig,
- hardlywigheid,
- nasopharyngitis,
- braking,
- infeksies van die asemhalingstelsel.
As u die middel gebruik, is dit nodig om die aanbevelings in die instruksies streng te volg, u kan dit nie neem as u ten minste een van die kontraindikasies het nie. As vergiftiging of oordosis plaasvind as gevolg van die gebruik van die middel, moet u onmiddellik 'n ambulans skakel, aangesien hierdie negatiewe verskynsels aansienlike gesondheidsprobleme kan veroorsaak wat selfs tot die dood kan lei.
Beginsels en metodes vir die opsporing van diabetes
Vir die behandeling van gewrigte het ons lesers DiabeNot suksesvol gebruik. Aangesien die produk gewild is, het ons besluit om dit onder u aandag te bring.
Diagnose van diabetes mellitus bestaan uit 'n uitgebreide ondersoek, die nodige toetse en die ondersoek deur 'n dokter deur 'n endokrinoloog. Dit is gewoonlik nie moeilik om so 'n diagnose te maak nie, aangesien baie pasiënte reeds met 'n lopende siekte kliniek toe gaan.
Maar moderne navorsingsmetodes kan nie net die aanvanklike, verborge stadiums van suikersiekte herken nie, maar ook die toestand wat hierdie siekte voorafgaan, wat prediabetes genoem word of 'n skending van die verdraagsaamheid teenoor koolhidrate.
Kliniese diagnostiese metodes
Die dokter versamel 'n anamnese, identifiseer risikofaktore, oorerflikheid, luister na klagtes, ondersoek die pasiënt, bepaal sy gewig.

Simptome wat in ag geneem word by die diagnose van diabetes:
- sterk konstante dors - polydipsie,
- oormatige urienvorming - poliurie,
- gewigsverlies met verhoogde eetlus - tipies vir tipe 1-diabetes,
- vinnige, beduidende gewigstoename - tipies vir tipe 2-diabetes,
- sweet, veral na eet,
- algemene swakheid, moegheid,
- ernstige jeuk van die vel wat met niks tevrede is nie,
- naarheid, braking,
- aansteeklike patologieë, soos pustulêre velsiektes, gereeld sproei in die mond of vagina, ens.
Dit is nie nodig dat 'n persoon al die geïnduseerde simptome het nie, maar as daar ten minste 2-3 waargeneem word, is dit die moeite werd om die ondersoek voort te sit.
Daar moet op gelet word dat met tipe 1-diabetes alle simptome vinnig ontwikkel en die pasiënt die presiese datum van die aanvang van simptome kan onthou, en sommige pasiënte word so onverwags dat hulle in intensiewe sorg beland in 'n toestand van diabetiese koma. Pasiënte met hierdie tipe diabetes is gewoonlik mense onder 40-45 jaar of kinders.
Die latente kursus is meer kenmerkend van tipe 2-diabetes mellitus, daarom sal ons die diagnose van hierdie spesifieke vorm van koolhidraatmetabolisme-afwyking verder bespreek.
Van groot belang vir die diagnose van tipe 2-diabetes is risikofaktore, wat die volgende insluit:
- ouderdom van 40-45 jaar oud,
- prediabetes of verswakte glukosetoleransie,
- oorgewig, vetsug (BMI ouer as 25),
- verhoogde bloedlipiedprofiel,
- hoë bloeddruk, bloeddruk bo 140/90 mm RT. Art.,
- lae liggaamlike aktiwiteit
- vroue wat in die verlede 'n afwyking van koolhidraatmetabolisme tydens swangerskap gehad het of 'n kind gebore het wat meer as 4,5 kg weeg,
- polisistiese eierstok.
Alle persone ouer as 40-45 jaar moet een keer per jaar op hoë bloedsuiker ondersoek word, en mense met vetsug en met die teenwoordigheid van ten minste een risikofaktor - een keer per jaar.
In die opkoms van tipe 2-diabetes speel oorerflikheid 'n belangrike rol. Die bestaan van hierdie siekte by familielede verhoog die kanse om tipe 2-diabetes te ontwikkel. Statistiek sê dat iemand met 'n ouer wat diabeet het, ook in 40% van die gevalle siek sal word.
Dosisvorm
Filmbedekte tablette 25 mg, 50 mg of 100 mg
Een tablet bevat
aktiewe stof - sitagliptienfosfaatmonohydraat 32,13 mg, 64,25 mg of 128,5 mg (gelykstaande aan 25 mg, 50 mg of 100 mg sitagliptien),
hulpstoffen: mikrokristallyne sellulose, kalsiumwaterstoffosfaat (watervry), ongemaalde, croscarmellose-natrium, magnesiumstearaat, natriumstearielfumarat,
filmbedekking samestelling Opadray® II Pink 85F97191 (vir 'n dosis van 25 mg), Opadray® II Ligte beige 85F17498 (vir 'n dosis van 50 mg), Opadray® II Beige 85F17438 (vir 'n dosis van 100 mg): polivinielalkohol, titaandioksied E171, makrogol / poliëtileenglikol 3350, talk, yster (III) oksied geel E172, yster (III) oksied rooi E172.
25 mg tablette - Die tablette is ronde, tweekleurige, bedek met 'n pienk filmomhulsel, met '221' aan die een kant gegraveer en aan die ander kant glad.
50 mg tablette - Die tablette is ronde, tweekleurige, bedek met 'n filmmembraan van 'n ligte beige kleur, met die graafwerk "112" aan die een kant en glad aan die ander kant.
100 mg tablette - Die tablette is ronde, tweekleurige, bedek met 'n beige filmskulp, aan die een kant met '277' gegraveer en aan die ander kant glad.
Laboratoriumnavorsingsmetodes
Vir die diagnose van tipe 2-diabetes word verskillende soorte toetse gebruik. Sommige tegnieke word as vertonings gebruik. Screening is 'n studie wat daarop gemik is om die siekte in die vroeë stadiums te identifiseer, uitgevoer deur 'n groot aantal mense wat dikwels nie duidelike simptome van die siekte het nie. Die bepaling van glikosileerde hemoglobien is die mees betroubare metode om diabetes te diagnoseer.
Glikosileerde hemoglobien is die eritrosiete hemoglobien wat 'n glukosemolekule aangeheg het.Die mate van glukosilering hang af van die konsentrasie van glukose in die bloed, wat in eritrosiete onveranderd bly gedurende hul leeftyd van drie maande. Die norm van geglokosileerde hemoglobien is 4,5-6,5% van die totale hoeveelheid hemoglobien.
In hierdie verband weerspieël die persentasie sulke hemoglobien te eniger tyd die gemiddelde bloedsuikervlak van die pasiënt vir 120 dae voor die studie. Dit help nie net om latente tipe 2-diabetes mellitus te openbaar nie, maar ook om die mate van siektebeheer te bepaal en die toereikendheid van terapie te evalueer.

Metodes vir die opsporing van suikersiekte word in basiese en aanvullende verdeel.
Die belangrikste metodes sluit die volgende in:
- bepaling van bloedsuikervlak, uitgevoer: op 'n leë maag, 2 uur na eet, voor slaaptyd,
- 'n studie van die hoeveelheid glykosileerde hemoglobien,
- glukosetoleransietoets - tydens die studie drink die pasiënt 'n sekere hoeveelheid glukose en skenk hy bloed voor die vinger van die vinger en 2 uur nadat hy die diagnostiese cocktail geneem het. Hierdie toets help om die tipe koolhidraatmetabolisme-afwyking duidelik te maak, en kan u prediabetes van ware diabetes onderskei,
- bepaling van die teenwoordigheid van suiker in die urine - glukose gaan in die urine wanneer die konsentrasie meer as 8-9 bepaal,
- ontleding van die vlak van fruktosamien - stel u in staat om die suikervlak gedurende die afgelope 3 weke uit te vind,
- studies oor die konsentrasie van ketone in urine of bloed - bepaal die akute aanvang van diabetes of die komplikasies daarvan.
Bykomende metodes word genoem om die volgende aanwysers te bepaal:
- bloedinsulien - om die sensitiwiteit van liggaamsweefsel vir insulien te bepaal,
- outo-antiliggame teen pankreasselle en insulien - toon 'n outo-immuun oorsaak van diabetes,
- proinsulien - vertoon die funksionaliteit van die pankreas,
- ghrelin, adiponektien, leptien, resistien - aanduiders van die hormonale agtergrond van vetweefsel, beoordeling van die oorsake van vetsug,
- C-peptied - stel u in staat om die tempo van selleverbruik deur selle uit te vind,
- HLA-tik - word gebruik om genetiese patologieë te identifiseer.
Hierdie metodes word gebruik in die geval van probleme tydens die diagnose van die siekte by sommige pasiënte, asook vir die keuse van terapie. Die aanstelling van addisionele metodes word uitsluitlik deur die dokter bepaal.
Farmakologiese eienskappe
farmakokinetika
Na orale toediening van 100 mg sitagliptien word die maksimum konsentrasie (Cmax) bereik tussen 1 en 4 uur vanaf die tyd van toediening. Die oppervlakte onder die konsentrasie-tydkurwe (AUC) neem toe in verhouding tot die dosis en beloop 8,52 μmol · uur, indien 100 mg oraal ingeneem word, Cmax is 950 nmol, die halfleeftyd (T1 / 2) is 12,4 uur. Die plasma AUC van sitagliptien het met ongeveer 14% gestyg na die volgende dosis van 100 mg van die geneesmiddel na die bereiking van die ewewigstoestand na die neem van die eerste dosis. Die intra- en inter-individuele AUC-veranderlikheidskoëffisiënte van sitagliptien is onbeduidend (5,8% en 15,1%). Die farmakokinetika van sitagliptien in die algemeen by gesonde individue en pasiënte met tipe 2-diabetes is soortgelyk. Absorpsie. Die absolute biobeskikbaarheid van sitagliptien is ongeveer 87%. Aangesien die gesamentlike inname van sitagliptien en vetterige voedsel nie die farmakokinetika beïnvloed nie, kan die medisyne voorgeskryf word, ongeag die ete.
Verspreiding. Die gemiddelde verspreidingsvolume in ewewig na die inname van 'n enkele dosis van 100 mg sitagliptien is ongeveer 198 L. Die sitagliptienfraksie wat aan plasmaproteïene bind, is relatief laag, op 38%.
Metabolisme. Slegs 'n klein fraksie van die geneesmiddel wat in die liggaam ontvang word, word gemetaboliseer. Ongeveer 79% van sitagliptien word onveranderd in die urine uitgeskei. Ongeveer 16% van die middel word in die vorm van sy metaboliete uitgeskei.Spore van ses metaboliete is gevind wat waarskynlik nie die aktiwiteit van die remmende effek van sitagliptien DPP-4 in plasma beïnvloed het nie. Die primêre ensiem wat by die beperkte metabolisme van sitagliptien betrokke was, is gevind dat dit CYP3A4 is wat CYP2C8 insluit.
Onttrekking. Na orale toediening van 14C-gemerkte sitagliptien deur gesonde vrywilligers, is ongeveer 100% van die middel 1 week uitgeskei met ontlasting en urine van onderskeidelik 13% en 87%. Die gemiddelde eliminasie-halfleeftyd vir orale toediening van 'n enkele dosis van 100 mg sitagliptien is ongeveer 12,4 uur; nieropruiming is ongeveer 350 ml / min.
Die uitskeiding van sitagliptien word hoofsaaklik uitgevoer deur die niere deur die niere te skei deur die meganisme van aktiewe buisafskeiding. Sitagliptin is 'n substraat vir die vervoerder van tipe III organiese menslike anione (hOAT-3), wat betrokke kan wees by die uitskeiding van sitagliptien deur die niere. Die betrokkenheid van hOAT-3 by die vervoer van sitagliptien is nog nie klinies bestudeer nie. Sitagliptien is ook 'n substraat van p-glykoproteïen, wat ook betrokke kan wees by die eliminasie van sitagliptien in die nier. Siklosporien, 'n remmer van p-glikoproteïen, verminder egter nie die renale klaring van sitagliptien nie. Sitagliptin is nie 'n substraat vir 'n organiese kationiese vervoerder (OCT2), 'n organiese anioniese vervoerder (OAT1) of proteïentransporter nie (PEPT1 / 2).
In studies invitro, sitagliptien belemmer nie OAT3 (IC50 = 160 μM) of p-glikoproteïen (tot 250 μM) bemiddelde oordrag by terapeuties beduidende plasmakonsentrasies nie. In kliniese studies het sitagliptien weinig invloed op plasmakonsentrasies van digoksien, maar sitagliptien kan 'n ligte remmer van p-glikoproteïen wees.
Pasiënte met nierversaking. In pasiënte met ligte nierversaking (kreatinienopruiming KK 50-80 ml / min) was daar geen klinies beduidende toename in die konsentrasie van sitagliptien in bloedplasma in vergelyking met die kontrolegroep van gesonde vrywilligers nie. 'N Ongeveer 2-voudige toename in AUC vir sitagliptien is waargeneem by pasiënte met matige nierversaking (CC 30-50 ml / min), 'n viervoudige toename in AUC is waargeneem by pasiënte met ernstige nierversaking (CC minder as 30 ml / min) en pasiënte met n stadium van nierversaking wat met hemodialise was, in vergelyking met die kontrolegroep. Daarom is dosisaanpassing nodig om 'n terapeutiese konsentrasie van die middel in bloedplasma by pasiënte met matige tot ernstige nierinsufficiëntie te verkry. Sitagliptien word in 'n klein mate uitgeskei tydens hemodialise (13,5% van die dosis vir 'n 3-4 uur dialisesessie, wat 4 uur na die gebruik van die middel begin is).
Pasiënte met lewerversaking. In pasiënte met matige leverinsufficiëntie (7-9 punte op die Child-Pugh-skaal) is dosisaanpassing nie nodig nie. Daar is geen kliniese gegewens oor die gebruik van sitagliptien by pasiënte met ernstige leverinsufficiëntie nie (meer as 9 punte op die Child-Pugh-skaal). Aangesien sitagliptien hoofsaaklik deur die niere uitgeskei word, moet 'n mens nie 'n noemenswaardige verandering in die farmakokinetika van sitagliptien verwag by pasiënte met ernstige leverfunksie.
Ouderdom. Afhangend van die ouderdom is daar geen dosisaanpassing nodig nie. By bejaarde pasiënte (65-80 jaar) is die plasmakonsentrasie van sitagliptien 19% hoër as by jonger pasiënte.
Kinders. Ondersoeke oor die gebruik van sitagliptien by kinders is nog nie gedoen nie.
Geslag, ras, liggaamsmassa-indeks. Dit is nie nodig om die dosis van die middel aan te pas nie, afhangende van geslag, ras of BMI. Hierdie eienskappe het nie 'n klinies beduidende effek op die farmakokinetika van sitagliptien gehad nie.
Tipe 2-diabetes. Die farmakokinetika van sitagliptien is oor die algemeen dieselfde by gesonde individue en pasiënte met tipe 2-diabetes. Uit kliniese studies is bevind dat geslag, ras en liggaamsgewig nie 'n beduidende kliniese effek op die farmakokinetika van sitagliptien het nie.
farmakodinamika
Januvia is 'n lid van die klas mondelinge hipoglykemiese middels, dipeptidyl peptidase 4 (DPP-4) remmers, wat die glukemiese beheer by pasiënte met tipe 2-diabetes verbeter deur die aktiewe hormone van die inkretienfamilie te verhoog. Hormone van die inkretienfamilie, insluitend glukagon-agtige peptied-1 (GLP-1) en glukose-afhanklike insulinotropiese peptied (HIP), word gedurende die dag in die ingewande afgeskei, en hul vlak neem toe in reaksie op voedselinname. Die inkretiene vorm deel van die interne fisiologiese stelsel vir die regulering van glukose-homeostase. Met normale of verhoogde bloedglukosevlakke, dra die hormone van die inkretienfamilie by tot 'n toename in insulien sintese, sowel as die afskeiding daarvan deur pankreas beta-selle as gevolg van die signalering van intrasellulêre meganismes geassosieer met sikliese AMP (adenosien monofosfaat).
Studies van GLP-1- of DPP-4-remmers in dieremodelle met tipe 2-diabetes het getoon dat verbeterde glukose-sensitiwiteit van ß-selle en die stimulering van insulinsintese gestimuleer is. Daar was 'n toename in glukose-absorpsie met 'n toename in insulienproduksie. GLP-1 help ook om die verhoogde afskeiding van glukagon deur alfa-selle in die pankreas te onderdruk. 'N Afname in glukagonkonsentrasie teen die agtergrond van 'n toename in insulienvlakke dra by tot 'n afname in glukoseproduksie deur die lewer, wat uiteindelik lei tot 'n afname in glukemie.
By 'n lae konsentrasie bloedglukose word die genoemde effekte van inkretiene op insulienvrystelling en 'n afname in glukagon-sekresie nie waargeneem nie. Die effek van stimulasie van GLP-1 en GUI hang af van die vlak van glukose in die bloed. Daar is geen stimulering van insulienproduksie of onderdrukking van die produksie van glukagon GLP-1 met 'n lae glukose in die bloed nie. GLP-1 en HIP stimuleer die produksie van insulien slegs as die bloedglukosevlak die norm begin oorskry. GLP-1 en HIP beïnvloed nie die vrystelling van glukagon in reaksie op hipoglukemie nie. Onder fisiologiese toestande word die werking van inkretiene beperk deur die ensiem DPP-4, wat incretiene vinnig hydroliseer met die vorming van onaktiewe produkte.
Januvia voorkom die hidrolise van inkretiene deur die ensiem DPP-4, waardeur die plasmakonsentrasies van die aktiewe vorme van GLP-1 en HIP verhoog word. Deur die verhoog van die inkretiene te verhoog, verhoog Januvia die glukose-afhanklike vrystelling van insulien en help dit om die afskeiding van glukagon te verminder. By pasiënte met tipe 2-diabetes mellitus met hiperglykemie lei hierdie veranderinge in die afskeiding van insulien en glukagon tot 'n afname in die vlak van geglokosileerde hemoglobien НbА1С en 'n afname in die plasmakonsentrasie van glukose, bepaal op 'n leë maag en na 'n stresstoets. Die glukose-afhanklike effek van sitagliptien verskil van die effekte van sulfonylureum, wat insulienvrystelling verhoog selfs by lae glukosevlakke en kan lei tot hipoglisemie by pasiënte met tipe 2-diabetes en gesonde persone. Sitagliptin is 'n uiters selektiewe remmer van die ensiem DPP-4, en by terapeutiese konsentrasies belemmer dit nie nouverwante ensieme DPP-8 of DPP-9 nie.
Samevatting van 'n wetenskaplike artikel oor medisyne en gesondheidsorg, skrywer van 'n wetenskaplike werk - Kim S.S., Kim Yin Zhuo, Lee K.D., Park C.H., Kim Y.I., Lee Y.S., Chung S.Ch. ., Lee S.Ch.
Vir die behandeling van tipe 2-diabetes mellitus (T2DM) word die vroeë begin van kombinasie-behandeling met hipoglisemiese middels aanbeveel. In 'n multisentrum, dubbelblinde, gerandomiseerde proef in parallelle groepe, is die effektiwiteit en veiligheid van sitagliptien en metformien as 'n vaste kombinasie (Sit / Met) vergelyk met glimepiride as die aanvanklike behandeling vir pasiënte met tipe 2-diabetes. Metodes. Pasiënte met T2DM (ouer as 18 jaar) is gerandomiseer om binne 30 weke na die aanvanklike uitwasperiode Sith / Met of glimepiride te ontvang.Die primêre eindpunt was die verandering in HbA1-vlak vanaf die basislyn. Sekondêre eindpunte bevat data van pasiënte wat die doelwit bereik het om glimpiried HbA1c te behandel (n = 145). Na 30 weke van behandeling het die Sit / Met-kombinasie die glimepiried oorskry om die vlak van HbA1c te verlaag (onderskeidelik 1,49 en 0,71%), die intergroepverskil van 0,78%, glimpiried (40,1%, p glimepiried) (verskil in die gemiddelde reeks van 23,5 mg / dl, p van hipoglukemie en gewigstoename was statisties beduidend laer in die Sit / Met-groep in vergelyking met glimepiride (5,5% vergeleke met 20,1%, 0,83 kg in vergelyking met +0,90 kg, onderskeidelik vir van beide vergelykings, die waarde van p met glimepiride, die aanstelling van Sit / Met as die aanvanklike terapie 30 weke na die aanvang van die studie het meer 'n duidelike verbetering in glukemiese beheer en liggaamsgewig, terwyl die voorkoms van hipoglukemie daal.
Teks van 'n wetenskaplike artikel oor die onderwerp "Die effektiwiteit en veiligheid van 'n vaste kombinasie van sitagliptien / metformien in vergelyking met glimepiride by pasiënte met tipe 2-diabetes mellitus: 'n multisentrum-gerandomiseerde dubbelblinde studie"
Doeltreffendheid en veiligheid van 'n vaste kombinasie van sitagliptien / metformien in vergelyking met glimepiride by pasiënte met tipe 2-diabetes mellitus: multisentrum-gerandomiseerde dubbel
Kim S. SL 2, Kim I. CHL 2, Lee C.D. 3, Park C. H. 4, Kim Y.I. 5, Lee Y.S. 7, Chung S. Ch. 6, Lee S. Deel 8
1 Departement Endokrinologie en Metabolisme, Afdeling Terapie, Busan State University Hospital, Suid-Korea
2 Instituut vir Biomediese Navorsing, Busan State University Clinic, Suid-Korea
3 Departement Endokrinologie en Metabolisme, Departement Terapie, Daedong-hospitaal, Suid-Korea
4 Departement Endokrinologie en Metabolisme, Departement Terapie, Busan Peck-hospitaal, Universiteit van Inje, College of Medicine, Universiteit van Inje, Busan, Suid-Korea
5 Departement Endokrinologie en Metabolisme, Afdeling Terapie, Ulsan Universiteitshospitaal, Suid-Korea
6 Departement Endokrinologie en Metabolisme, Departement Terapie, Dongkang Mediese Sentrum, Suid-Korea
7 Departement Endokrinologie en Metabolisme, Departement Terapie, Dongguk Universiteitskollege vir Geneeskunde, Gyeongju, Suid-Korea
8 MSD Korea Bpk., Seoel, Suid-Korea
Vir die behandeling van tipe 2-diabetes mellitus (T2DM) word die vroeë begin van kombinasie-behandeling met hipoglisemiese middels aanbeveel. In 'n multisentrum, dubbelblinde, gerandomiseerde proef in parallelle groepe, is die effektiwiteit en veiligheid van sitagliptien en metformien as 'n vaste kombinasie (Sit / Met) vergelyk met glimepiride as die aanvanklike behandeling vir pasiënte met tipe 2-diabetes.
Metodes. Pasiënte met T2DM (ouer as 18 jaar) is gerandomiseer om Sith / Met of glimepiride vir 30 weke na die aanvanklike uitwasperiode te ontvang. Die primêre eindpunt was die verandering in HbA1-vlak vanaf die basislyn. Sekondêre eindpunte het pasiëntdata ingesluit
* Hierdie artikel is in die openbaar beskikbaar in ooreenstemming met die bepalings van die nie-kommersiële lisensie Creative Common Attribution, wat u toelaat om data op enige manier te gebruik, versprei en weer te gee, mits daar na die oorspronklike werk behoorlik verwys word.
HbA1c behandelingsverskaffers i Kan u nie vind wat u nodig het nie? Probeer die literatuurkeusediens.
8 MSD Korea Bpk., Seoel, Suid-Korea, Suid-Korea
Vir die behandeling van tipe 2-diabetes (T2D) word vroeë aanvang van kombinasie-behandeling met anti-hiperglikemiese middels aanbeveel. Die huidige multisentrum-dubbelblinde gerandomiseerde parallelgroepstudie het die effektiwiteit en veiligheid van 'n kombinasie met vaste dosis sitagliptien en metformien (Sita / Met) ondersoek in vergelyking met glimepiride in T2D-pasiënte as aanvanklike behandeling.
Metodes. Pasiënte van tipe 2-diabetes (ouderdomme> 18 jaar) is na 'n inloopperiode na Sita / Met of glimepiride vir 30 weke gerandomiseer. Die primêre eindpunt was verandering vanaf basislyn (CFB) in HbA1c. Sekondêre eindpunte het die deel van pasiënte wat die doelwit HbA1c bereik het, ingesluit
Gevolgtrekkings. In vergelyking met gLimepiride het Sita / Met as 'n aanvanklike behandeling gelei tot 'n aansienlike groter verbetering in glukemiese beheer en liggaamsgewigveranderinge, met 'n laer voorkoms van hipoglukemie, gedurende 30 weke.
glimepiride, hipoglykemie, metformien, sitagliptienfosfaat
J Diabetes. 2017, 9: 412-422. doi: 10.1111 / 1753-0407.12432
Die kliniese en ekonomiese las van diabetes en die behandeling daarvan hou steeds 'n groot probleem in vir die mediese gemeenskap 1, 2. Die algemene voorkoms van diabetes in 2014 onder volwassenes was 9%, 90% van hierdie gevalle is tipe 2-diabetes (T2DM ). Volgens Suid-Korea, in 2011, volgens die nasionale gesondheids- en voedingsverifiëringsprogram.die beraamde voorkoms van diabetes mellitus by pasiënte ouer as 30 jaar was 10,5% gebaseer op slegs inligting oor vastende plasmaglukose (GF) en 12,4% gebaseer op data op die vlak van GF en HbA1c.
Vir diabetes mellitus is daar 'n sterk korrelasie van die teenwoordigheid van die siekte met die ontwikkeling van mikro- en makrovaskulêre komplikasies wat lei tot skade aan organe en weefsels. Hierdie komplikasies word by 30-50% van die pasiënte aangeteken, en hul risiko is grootliks geassosieer met voorheen geïdentifiseerde hipoglukemie. Aangesien glukemiese terapie hoofsaaklik op die voorkoming van mikrovaskulêre komplikasies gerig is, is die verhouding tussen glukemiese beheer en makrovaskulêre komplikasies 7–9 effens swakker. Nietemin, die voordeel van die bereiking van intensiewe glukemiese beheer in die vroeë stadiums van diabetesbehandeling is die moontlikheid om beheer vir 'n dekade of meer selfs met minder intensiewe verdere behandeling 10, 11. te handhaaf. Hierdie onlangse bevindings ondersteun 'n verandering in behandelingsbeginsels om vroeëre bereiking van glukemiese doelstellings in pasiënte met tipe 2-diabetes.
Die behandelingsalgoritme ontwikkel deur die Amerikaanse Vereniging van Kliniese Endokrinoloë (AACE) beveel die vroeë aanvang van metformienkombinasie-terapie aan met 'n aanvanklike HbA1c-vlak> 7.5% (58 mmol / mol), aangesien 'n HbA1c-vlak van 9.0% (75 mmol / mol) bereik is, aangesien dit onwaarskynlik is dat hierdie pasiënte die teikenvlak van HbA1c met monformering met metformien sal bereik. Dus, die vroeë aanvang van gekombineer
terapie met hipoglykemiese middels met verskillende werkingsmeganismes kan 'n besondere effektiewe opsie wees vir pasiënte met tipe 2-diabetes.
In die huidige kliniese praktyk word sulfonielureumderivate 17-19 dikwels gebruik as aanvanklike terapie om insulienafskeiding te stimuleer by pasiënte met tipe 2-diabetes. Weens die vermoë om insulienafskeiding te verbeter (wat 'n bekende probleem in T2DM is), is glimepiride in baie lande, insluitend Korea, as eerste-lyn monoterapie gebruik. Vanweë die hoër snelheid van die algehele sterftes in vergelyking met metformien, het die besorgdheid oor die veiligheid van sulfonielureumderivate 20, 21 nietemin ontstaan. Daarbenewens word die ontwikkeling van hipoglukemie en 'n toename in liggaamsgewig opgemerk met die gebruik van glimepiride. Sitagliptin, 'n orale, sterk selektiewe dipeptidylpeptidase-remmer (DPP), was die eerste geregistreerde middel in hierdie klas om volwasse pasiënte met tipe 2-diabetes te behandel. Sitagliptien verhoog insulienafskeiding en verminder glukagonkonsentrasie via 'n hormoon-nuwe seinweg. Die werking van hierdie middel hang af van die glukosevlak 23, 24. Daar is aangetoon dat sinergieë, hoë effektiwiteit en goeie verdraagsaamheid van die kombinasie van sitagliptien en metformien (Sit / Met) by pasiënte. met T2DM 25, 26. Daar is egter voorheen geen studies oor die vaste kombinasie Sit / Met in Korea gedoen nie.
Die doel van die voorgestelde studie in Korea was om die effektiwiteit en veiligheid van die aanvanklike Sit / Met FDC-terapie te bestudeer in vergelyking met glimepiride by pasiënte met tipe 2-diabetes.
Die aangebied multisentrum-gerandomiseerde dubbelblinde studie in parallelle groepe is vanaf 6 Mei 2010 tot 29 Oktober 2013 gedurende 39 weke in 21 kliniese sentrums van Suid-Korea uitgevoer (identifikasienommer CLinicaLtriaLs.gov Ш: NCT00993187, protokol van die Merk-maatskappy MK-0431A -202). Pasiënte is 1: 1 gerandomiseer vir 'n 30-week-terapie na 'n opsionele periode van 6 weke / inwasperiode en 'n verpligte induksieperiode van 2 weke vir blinde placebo-terapie (Fig. 1, A). Hierdie studie is uitgevoer in ooreenstemming
Fig. 1. Bestudeer Ontwerp en verspreiding van pasiënte
A - gedetailleerde inligting oor die verspreiding van pasiënte, B - Sit / Met EyO - sitagliptien en metformien in 'n vaste kombinasie, AE - 'n ongewenste verskynsel, SNA - 'n ernstige ongewenste verskynsel.
* Die kliniese navorsingsentrum is gesluit omdat die navorser uit eie vrye wil ontslaan is en dit onmoontlik was om die pasiënt na 'n ander kliniese sentrum oor te plaas. Die borg het besluit om hierdie kliniese sentrum te sluit en die pasiënt uit te sluit gedurende die keuringstydperk vir die kliniese studie.
met die standaarde van die Reëls vir die uitvoering van kliniese proewe van gehalte, die bepalings van die Helsinki-verklaring en toepaslike staats- en / of plaaslike wette en regulasies. Voor die studie is goedkeuring deur 'n onafhanklike etiekkomitee in elke navorsingsentrum verkry, sowel as 'n skriftelike ingeligte toestemming van elke pasiënt.
volgens die navorsingsvereistes of stel die pasiënt aan die risiko bloot volgens die navorser of mediese waarneming. Pasiënte is uitgesluit van die studie tydens die inleidende periode van placebo of tydens randomisering indien die vlak van GPN of die resultate van 'n ontleding van die vasende kapillêre bloedglukose in 'n kliniese sentrum onderskeidelik minder as 110 mg / dl of hoër as 300 mg / dl was.
Die aanvanklike inleidingsperiode het volwasse pasiënte (> 18 jaar oud) met T2DM ingesluit wat nie swanger was nie, nie borsvoed nie, en vir wie daar 'n buitengewone kans op bevrugting was gedurende die studie of periode van kliniese waarneming. Die keuringskriteria tydens die keuringsbesoek het 'n HbA1c-vlak ingesluit van> 7.0 (53 mmol / mol) tot 6.5 (48 mmol / mol) tot 7.0 (53 mmol / mol) tot 14 dae, immunomodulerende middels, chirurgie vir algemene narkose (binne dertig dae voor die aanvang van die studie of beplande intervensies), asook enige opsies vir eksperimentele terapie (binne 8 weke voor die aanvang van die studie).
Ander uitsluitingskriteria sluit in hipersensitiwiteit of kontraindikasies vir die gebruik van sulfonielureumderivate, DPP-4-remmers of biguaniede, serumkreatinien> 1,5 mg / dl by mans en> 1,4 mg / dl by vroue, trigliseriede bo 500 mg / dl, wanbalans van tiroïedstimulerende hormoon, lewersiekte in die aktiewe fase (behalwe vir vetterige hepatose), kardiovaskulêre siektes, 'n positiewe resultaat van 'n ontleding van die menslike immuniteitsgebreksvirus, afwykings van die hematopoietiese stelsel, 'n geskiedenis van kwaadaardige neoplasmas, 'n positiewe urien-swangerskapstoets, liggaamsmassa-indeks (BMI)> 35 kg / m2, of toestande wat kan lei tot nie-nakoming
Gedurende die inleidings- / uitwasperiode is pasiënte in kennis gestel oor dieet en oefening, en die instruksie gegee oor die gebruik van bloedglukosemeters. Gedurende die placebo-periode het pasiënte placebo-tablette geneem wat ooreenstem met Sit / Met in 'n vaste kombinasie (FDC) 50/500 mg (1 tablet gedurende die oggend- en aandmaaltye), in kombinasie met 'n placebo-tablet wat ooreenstem met 1 mg glimepiride (1 keer per dag tot die oggendmaal).
Gedurende die behandelingstyd het die eksperimentele groep Sit / Met in 'n vaste kombinasie geneem (Yanumet, Merck & Co., Inc., West Point, PA, VSA) 50/500 mg 2 keer per dag mondelings tydens etes met 'n dosis titrasie van tot 50 / 1000 mg 2 keer per dag vir 'n periode van 4 weke. Tot die 8ste week na die aanvanklike periode van 4 weke, is titrasie toegelaat met 'n dosisverlaging van Sit / Met FDC in geval van onverdraagsaamheid, en geen dosisveranderings is toegelaat nie. Placebo-tablette wat ooreenstem met glimepiride (Merck & Co., Inc., InvaGen Pharmaceuticals, Happodge, New York, VSA) moet een keer per dag geneem word. Pasiënte van die kontrolegroep het glimepiried ontvang in 'n aanvanklike dosis van 1 mg / dag met 'n titrasie van tot 6 mg / dag vir die eerste 8 weke volgens die oordeel van die navorser, volgens die aanbevelings van die ADA (American Diabetes Association, American Association of Diabetologists). Placebo-tablette wat ooreenstem met Sit / Met FDC, moes twee keer per dag geneem word.Om 'n blinde regimen te verseker, is 'n benadering met twee soorte placebo gebruik: (1) pasiënte uit die Cit / Met FDC-groep het Cit / Met FDC 50/500 mg tablette en / of Sit / Met FDC 50/1000 mg en placebo-tablette ontvang wat ooreenstem met glimepiride, ( 2) pasiënte uit die glimepiriedgroep het 2 placebo-tablette ontvang wat ooreenstem met Sit / Met FDC 50/500 mg en / of Sit / Met FDC 50/1000 mg en glimepiride tablette (die dosis is bepaal op grond van titrasie) 1 of 2 mg.
Hou by die behandeling
Om aan die keuringskriteria gedurende die inleidende periode te voldoen, was 'n 85% -vlak van behandeling nodig (bereken op grond van die berekening van placebo-tablette wat in 'n eenvoudige blinde regimen geneem is). Die nakoming van terapie is gedurende die behandelingsperiode geëvalueer met behulp van die volgende formule: persentasie aanhegting = (werklike aantal behandelingsdae / vereiste aantal behandelingsdae) x 100.
Randomisering / verspreiding / blinde modus
Randomiseringskemas is opgestel deur 'n statistikus wat nie by die studie betrokke was nie. Aan die einde van die inleidingsperiode van placebo (besoek 5) het alle pasiënte wie se data aan die keuringskriteria voldoen, 'n aangrensende opdragnommer gekry van die toepaslike katalogus wat deur DreamCIS (Seoul, Korea) voorsien is. Blind-modus voorbereidings en verseëlde koeverte met kodes is verskaf deur Merck Sharp & Dohme (West Point, PA, VSA). Hierdie studie was dubbelblind, d.w.s. Navorsers, verpleegsters, aptekers en pasiënte het nie inligting oor die behandeling ontvang nie.
Evaluerings en prestasiekriteria
Evaluering van die hipoglykemiese effektiwiteit van terapie was gebaseer op die vlak van HbA1c, GPN en die vlak van verdraagsaamheid van die studiemiddel. Die primêre effektiwiteit eindpunt was die verandering in HbAlc-vlak vanaf basislyn in week 30 van terapie. Sekondêre eindpunte het veranderinge in GPN-vlakke van basislyn tot vlakke in week 30 ingesluit en die persentasie pasiënte wat 'n teiken HbA1c-vlak van minder as 7% (53 mmol / mol) in week 30 bereik het.
Die eindpunte van veiligheid sluit die voorkoms van hipoglukemie en veranderinge in liggaamsgewig vanaf die basislyn in. Algehele veiligheid en verdraagsaamheid is beoordeel aan die hand van die aantal behandelingsverwante nadelige gebeure (AE's), die resultate van 'n biochemiese bloedtoets (insluitend die vlak van alanien aminotransferase, aspartaat minotransferase, totale bilirubien en alkaliese fosfatase), hematologiese bloedtoets (insluitend algemene bloedtelling, leukosietformule en die absolute aantal neutrofiele), die belangrikste aanduiders van die toestand van die liggaam en algemene urienanalise.
Ongeveer 139 pasiënte in elke terapeutiese groep ('n totaal van 278 pasiënte) was nodig om die ware gemiddelde verskil van 0,4% van die verandering in HbA1c-vlak van die basis na die 30ste week van die behandeling tussen die Sit / Met FDC en glimepiride groepe met 'n bilaterale betekenisvlak te bepaal en 0,05. Hierdie berekening was gebaseer op 'n raming van die standaardafwyking (SD) van 1% om die verandering in HbA1c-vlak van die basislyn na die 30ste week van die behandeling te meet, met inagneming van die aanname van 90% krag en 5% van die pasiënte wie se data nie geëvalueer kan word nie.
'N Primêre eindpuntanalise om terapeutiese groepe te vergelyk om die meerderwaardigheid van een behandeling te bevestig, is uitgevoer met behulp van samevariansie-analise (ANCOVA) vir 'n volledige steekproef van pasiënte vir analise (FAS) met 'n p i-waarde. Kan u nie vind wat u benodig nie? Probeer die literatuurkeusediens.
Van die 628 pasiënte met tipe 2-diabetes wat getoets is vir deelname aan hierdie studie, is data uitgesluit; die oorblywende 292 is gerandomiseer (147 na die Sit / Met FDC-groep en 145 vir glimepiriedgroep). 229 pasiënte het die studie voltooi (sien Fig. 1, B). Die uitvalsyfer was 17,7% in die Sit / Met FDC-groep en 25,5% in die glimepiried-groep.
Basislynkenmerke was oor die algemeen vergelykbaar tussen die twee groepe (sien Tabel 1), met die uitsondering van 'n effens langer duur van T2DM in die Sit / Met FDC-groep (4.6 en 3.9 jaar).Die gemiddelde ouderdom van die pasiënte was onderskeidelik 54,8 en 53,1 jaar in die Sith / MetFDC en glimepiried groepe; die gemiddelde HbA1c vlak was 8,0% (64 mmol / mol) in die Sith / Met FDC groep en 8,1% (64 mmol / mol) in die glimepiriedgroep. Aanvanklik het 38,8 en 43,3% van die pasiënte nie voorheen hipoglikemiese terapie in onderskeidelik die Sit / Met FDC en glimepiride groepe ontvang nie. Inligting oor die neem van die dwelm
Tabel 1. Aanvanklike demografiese en kliniese kenmerke van pasiënte
I Indicator I Sit / Met FDC (n = 147) 1 Glimepiride (n = 145) 1 Totaal (n = 292) 1
Ouderdom, jare 54,8 ± 8,5 53,1 ± 9,2 53,9 ± 8,9
Geslag mans vroue 81 (55.1) 66 (44.9) 84 (57.9) 61 (42.1) 165 (56.5) 127 (43.5)
Liggaamsgewig, kg 67,3 ± 8,8 67,7 ± 10,4 67,5 ± 9,6
BMI, kg / m2 25,2 ± 2,7 25,0 ± 2,8 25,1 ± 2,7
Duur van tipe 2-diabetes mellitus, jare 4.6 ± 4.6 3.9 ± 3.7 4.2 ± 4.2
HbA1c% mmol / mol 8,0 ± 0,9 64,0 ± 9,8 8,1 ± 0,9 65,0 ± 9,8 8,0 ± 0,8 64,0 ± 8,7
GPN, mg / dl 171,5 ± 41,2 168,3 ± 39,4 169,9 ± 40,3
GFR 75,9 ± 11,7 76,7 ± 16,2 76,2 ± 13,3
Totale cholesterol, mg / dl 176,1 ± 34,9 171,0 ± 32,4 173,5 ± 33,7
LDL-cholesterol, mg / dl 97,3 ± 33,0 95,0 ± 28,1 96,2 ± 30,6
HDL-cholesterol, mg / dL 48,2 ± 11,0 48,8 ± 10,1 48,5 ± 10,5
Triglycerides, mg / dl 150,5 ± 88,2 134,1 ± 72,1 142,3 ± 80,8
TUIN, mmHg 125.3 ± 11.2 126.3 ± 13.2 125.8 ± 12.2
DBP, mmHg 76,7 ± 8,1 77,7 ± 8,5 77,2 ± 8,3
Vorige hipoglykemiese terapie Ja Nee 90 (61.2) 57 (38.8) 82 (56.6) 63 (43.4) 172 (58.9) 120 (41.1)
Vorige terapie 118 (80.3) 123 (84.8) 241 (82.5)
Hipolipidemiese middels 65 (44.2) 66 (45.5) 131 (44.9)
PAC-remmers 43 (29.3) 43 (29.7) 86 (29.5)
Medisyne teen bloedplaatjies 57 (38.8) 53 (36.6) 110 (37.7)
Noot. Tensy anders aangedui, is die data aangebied as gemiddelde ± standaardafwyking (By) of n (%). Sit / Met EyO - sitagliptien en metformien in 'n vaste kombinasie, DBP - diastoliese bloeddruk, GPN - vastende plasmaglukose, RAS - renien-angiotensienstelsel, CAD - sistoliese bloeddruk, BMI - liggaamsmassa-indeks, GFR - glomerulêre filtrasietempo, cholesterol LDL-cholesterol is 'n lae-digtheid lipoproteïne, HDL-cholesterol is 'n hoë-digtheid lipoproteïne cholesterol.
Tabel 2. Opsomming van maksimum, finale en gemiddelde dosis glimepiried
Aantal pasiënte met beskikbaar 141
Gemiddelde dosis ± RMS
afwyking (hey) 2.0 ± 1.3
Aantal pasiënte (%) met die maksimum
Die aantal pasiënte (%) met die finale dosis
80,3% van die pasiënte in die Sit / Met FDC-groep en 84,8% van die pasiënte in die glimepiriedgroep het die geskiedenis van die medisyne aangebied, die algemeenste genoemde lipiedverlagende medisyne, gevolg deur die frekwensie van antitrombotiese middels en medisyne wat die renien-angiotensienstelsel beïnvloed.
In beide groepe was daar 'n hoë vlak van behandeling (> 90%) onder pasiënte. Die meeste pasiënte het die studiemiddel langer as 24 weke geneem. Die gemiddelde duur van die geneesmiddel by enige dosis was in beide terapeutiese groepe soortgelyk (175,6 dae in die Sit / Met FDC-groep en 166,6 dae in die glimepiriedgroep).
Dosis titrasie in die glimepiried groep
Die gemiddelde voorgeskrewe dosis glimepiried was 2,0 mg (reeks: 1,0-6,0 mg). Die maksimum dosis van 1 mg is aan 46,1% (65/141) pasiënte toegewys, en slegs 17,7% (25/141) van die pasiënte het 'n maksimum dosis van 6 mg ontvang (tabel 2). Die finale dosis glimepiried was 1 mg in 49,6% (70/141) en 6 mg in 17,0% (24/141) van die pasiënte.
Prestasie-analise (FAS)
Primêre eindpunt
Op week 30 het die gemiddelde HbA1c-waarde van die aanvanklike waarde afgeneem: 8% (64 mmol / mol) tot 6,5%
Sitagliptin / Metformin FDC A
90 80 70 60 50 40 30 20 10
p i Kan u nie vind wat u nodig het nie? Probeer die literatuurkeusediens.
- Sitagliptin / Metformin FDC - Glimepiride
5 6 7 8 (0W) (2W) (4W) (8W)
- Sitagliptin / Metformin FDC - Glimepiride
Fig. 2. Effektiwiteits- en veiligheidsaanwysers gedurende die behandelingsperiode in die groepe sitagliptien en metformien in 'n vaste kombinasie (FDC) of glimepiride (A, B, G)
Veranderings in vergelyking met die aanvanklike waardes van (A) HbA1c van die volledige ontledingspopulasie (FAS), (B) vastende plasmaglukose (GPN) in FAS en (D) liggaamsgewig in die bevolking van pasiënte wat ten minste een dosis van die bestudeerde middel (APaT) ontvang het. Die persentasie pasiënte wat in week 30 (FAS) (B) die teiken HbA1c van 7 en 6,5% bereik het. Aantal pasiënte met ten minste 1 episode van hipoglukemie (APaT populasie) (D). Data is gemiddelde ± standaardfout van die gemiddelde (SEM) (B, D, D) of die gemiddelde ± SEM (A, C).
Verskil = -14,7% p i Kan u nie vind wat u benodig nie? Probeer die literatuurkeusediens.
In week 30 is die teiken HbA1 ^ vlak van minder as 7,0% (53 mmol / mol) behaal in 'n statisties beduidend groter deel van die pasiënte in die Sit / Met FDC groep
in vergelyking met die glimepiriedgroep (81,2 en 40,1%, p mediaan (36,5 maande)
Tyd geneem om diabetes te diagnoseer: mediaan (24,8 kg / m2) BMI: 65 jaar oud: mediaan (56 jaar) ouderdom: mediaan (7,8%)
■ Aanvanklike waarde HbA1c (%): i Kan u nie vind wat u benodig nie? Probeer die literatuurkeusediens.
■ Stratum: sonder hipoglisemiese middels
■ Stratum: die neem van hipoglisemiese middels
Fig. 3. Subgroepontleding
Die grafiek toon die verskille tussen behandelingsopsies (glimepiride minus sitagliptien met metagien in 'n vaste kombinasie) in verhouding tot die vlak van HbA1c in verskillende subgroepe, bepaal op grond van die aanvanklike demografiese en antropometriese eienskappe. In alle subgroepe van beide terapeutiese groepe is 'n beduidende afname vergeleke met die aanvanklike waarde waargeneem. In beide terapeutiese groepe, met hoër aanvanklike HbA1c-waardes, is 'n meer duidelike afname in hierdie aanwyser vanaf die aanvanklike vlak opgemerk. Intergroepverskille ten opsigte van veranderinge in die gemiddelde limiet vanaf basislyn na die dertigste week was oor die algemeen dieselfde in alle subgroepe wat geïdentifiseer is op grond van ouderdom, geslag, liggaamsmassa-indeks (BMI) en langer duur van tipe 2-diabetes mellitus.
Tabel 3. Opsomming van nadelige gebeure
Sif / Met FDC Glimepiride
(n = 146) (n = 144) glimepiride (95% CI +)
Dodelike uitkoms 0 (0) 0 (0)
Ernstige nadelige gebeure 8 (5.5) 9 (6.3) -0.8 (-7.7, 5.0)
Nadelige gebeure wat verband hou met die neem van die dwelm * 37 (25.3) 39 (27.1) -1,7 (-11.9.8.4)
Nadelige gebeure (pasiënte met> 1 voorkoms) 88 (60.3) 101 (70.1) -9.9 (-20.6, 1.1)
Nadelige gebeure tydens behandeling (> 5% van die pasiënte)
Gastro-intestinale afwykings 51 (34.9) 27 (18.8) 16.2 (6.0, 26.0)
Dyspepsie 19 (13.0) 9 (6.3)
Diarree 15 (10.3) 4 (2.8)
Naarheid 10 (6.8) 4 (2.8)
Buikpyn 4 (2.7) 0 (0.0)
Aansteeklike en parasitiese siektes 31 (21.2) 32 (22.2) -1.0 (-9.0, 11.0)
Nasofaryngitis 13 (8.9) 17 (11.8)
Infeksies in die boonste lugweë 12 (8.2) 4 (2.8)
Metaboliese en eetversteurings 14 (9.6) 33 (22.9) -13.3 (5.0, 22.0)
Hipoglukemie 8 (5.5) 29 (20.1)
Verlaagde eetlus 6 (4.1) 0 (0.0)
Die resultate van laboratorium- en instrumentele studies 8 (5.5) 15 (10.4) -4.9 (-1.0, 12.0)
Verhoogde bloedglukose 0 (0,0) 6 (4,2)
Oortredings van die senuweestelsel 14 (9.6) 9 (6.3) 3.3 (-10.0, 3.0)
Duiseligheid 5 (3.4) 2 (1.4)
Muskuloskeletale en bindweefselafwykings 10 (6.8) 11 (7.6) 2.0 (-7.0, 2.0)
Oortredings van die vel en onderhuidse weefsel 4 (2.7) 10 (6.9) -4.2 (-1.0, 10.0)
Staking van voorgeskrewe terapie as gevolg van nadelige gebeure 8 (5.5) 8 (5.6) -0.1 (-5.8, 5.6)
Staking van terapie as gevolg van terapie-verwante newe-gebeure. 7 (4.8) 3 (2.1) 2.7 (-1.8, 7.8)
Beëindiging van terapie as gevolg van ernstige nadelige gebeure 1 (0.7) 1 (0.7) 0
Noot. Tensy anders aangedui, word die aantal deelnemers in elke groep aangebied, word persentasies tussen hakies gegee. Alhoewel die pasiënt twee of meer nadelige gebeure kon ondervind, is die pasiëntgegewens in elke kategorie slegs 1 keer aangeteken. * Definieer deur die navorser as moontlik, waarskynlik of beslis verwant aan die toediening van medisyne. 95% vertrouensintervalle (CI) is volgens die metode van M1eSpep en IgtPep bereken. Sit / Met EyO, sitagliptin en metformien in 'n vaste kombinasie.
Vir ander aanwysers (vitale funksies, biochemiese ontleding van bloed, plasmalipiede of ander hematologiese parameters), is klinies beduidende veranderinge vanaf die aanvanklike vlak of verskille tussen die groepe nie aangeteken nie.
Die multisentrum-dubbelblinde studie in Koreaanse pasiënte met tipe 2-diabetes het die meerderwaardigheid van Sith / Met FDC bo glimepiried getoon ten opsigte van die verlaging van die HbA1c- en GPN-vlakke na 'n aanvanklike behandeling van 30 weke. 'N Teiken HbA1c-vlak van minder as 7,0% (53 mmol / mol) is behaal in 'n statisties beduidend groter deel van die pasiënte in die Sit / Met FDC-groep. Alhoewel beide behandelingsopsies glukemiese beheer verbeter het, het glimepiriedterapie tot 'n toename in liggaamsgewig gelei, terwyl met Sit / Met 'n geringe afname waargeneem is met minder uitgesproke hipoglukemie. Oor die algemeen is beide behandelingsopsies goed verdra.
Vir kombinasie-terapie met sitagliptien en metformien, is voorheen bewys dat effektiwiteit is ten opsigte van die bereiking van voldoende glukemiese
beheer, goeie verdraagsaamheid, 'n neutrale effek op liggaamsgewig en 'n lae risiko vir hipoglukemie 25, 26, 28. In die huidige studie is addisionele data verkry oor die gebruik van Sit / Met in 'n vaste kombinasie by pasiënte met tipe 2-diabetes. In ooreenstemming met die huidige kliniese praktyk in Korea, is glimepiride 'n eerste-middel middel vir tipe 2-diabetes. Die resultate van die huidige studie dui daarop dat Sit / Met FDC 'n voordeel het in die aanstelling van aanvanklike behandeling vir pasiënte met tipe 2-diabetes bo monoterapie met glimepiride. Gegewe die huidige aanbevelings oor die gebruik van kombinasieterapie in die vroeë stadiums van behandeling by pasiënte wat nie die teikenvlakke van HbA1c bereik nie, is hierdie resultate van groot kliniese belang vir die behandeling van suikersiekte in Korea.
In vorige studies wat die effektiwiteit en veiligheid van kombinasieterapie met sitagliptien en metformien in die Koreaanse bevolking geëvalueer het, is die effektiwiteit en goeie verdraagsaamheid van hierdie kombinasie bevestig. In 'n onlangse studie is die effektiwiteit van glukemiese beheer van metformien-gebaseerde kombinasieterapie vergelyk met sitagliptien, 'n sulfonielureumderivaat (glimepiride of
met gewysigde vrystellingsgliclazide) of pioglitazon by 116 pasiënte wat voorheen nie behandel is nie, is 'n soortgelyke glukemiese beheer van hierdie drie kombinasies in 'n wye reeks HbA1c-vlakke getoon. In 'n ander studie het Koreaanse pasiënte wat voorheen kombinasie-terapie (dubbel- of drievoudige kombinasie met metformien) ontvang het, 'n statisties beduidende verbetering in glukemiese beheer tydens behandeling met sitagliptien teen 'n dosis van 100 mg / dag. In die groep wat van glimepiried na sitagliptien oorgeskakel het, het die frekwensie van episodes van hipoglukemie verminder, en dus kan 'n soortgelyke behandelingsveranderingsopsie oorweeg word by pasiënte met herhalende vasende hipoglykemie. Ten spyte van die aangetoonde effektiwiteit van kombinasieterapie, was daar voorheen in Korea geen studies oor Sit / Met in 'n vaste kombinasie nie, en die voorgestelde studie is die eerste in sy soort.
Die voordelige effekte van die gebruik van vaste dosis-kombinasies is voorheen aangetoon vir ander tweekomponent-medisyne-kombinasies vir die behandeling van T2DM. In 'n gerandomiseerde, oop, multisenterstudie in parallelle groepe, het 209 Koreaanse pasiënte nie voldoende beheer van T2DM verkry nie, ten spyte van metformien monoterapie, was glimepiride / metformine FDC gebruik in lae dosisse of metformine dosis titrasie (binne 24 weke), glimepiride / metformin FDC het titrasie oorskry dosisse metformien in verhouding tot glukemiese beheer. Uit 'n empiries gesonde oorsig is die gevolgtrekking gekom dat metformien / pioglitazoon FDC doeltreffend is by pasiënte met insulienweerstandige diabetes, wat nie die doelstellings bereik het wat voldoen aan die aanbevole standaarde van mediese sorg tydens monoterapie nie. In 'n uitgebreide retrospektiewe analise van 'n databasis van 16.928 pasiënte, is dit gevind dat met rosiglitazoon / metformien FDC, daar 'n statisties beduidende verbetering was in die aanhang van die behandeling in vergelyking met behandelingsmetodes wat 2 medisyne bevat. Oor die algemeen kan die gebruik van FDC nie net die nakoming van terapie verbeter nie, maar ook 'n gunstiger verdraagsaamheidsprofiel hê, meer gemaklik wees vir pasiënte en 'n potensieel hoër koste-effektiwiteit hê. Die gebruik van Sit / Met FDC in die voorgestelde studie kan een van die faktore wees wat die hoë aanhang van behandeling beïnvloed het (
Byna 40% van die pasiënte wat by die studie ingesluit is, het nog nie voorheen hipoglisemiese behandeling ontvang nie. Die effektiwiteit van die aanvanklike behandeling met Sit / Met FDC by voorheen onbehandelde pasiënte is in verskeie vorige studies 35-37 beoordeel.Die effektiwiteit en veiligheid van Sit / Met FDC in vergelyking met pioglitazoon is onlangs in twee uitgebreide studies bestudeer wat ongeveer 500 pasiënte insluit, wat elk 'n statisties beduidende verbetering in glukemiese beheer met Sit / Met 35, 37 bevestig.
Van die pasiënte in die Sit / Met-groep is 'n afname in liggaamsgewig waargeneem, terwyl die liggaamsgewig by pasiënte uit die pioglitazon-groep toegeneem het. In 'n ander dubbelblinde, gerandomiseerde studie van 1250 voorheen onbehandelde pasiënte, het hulle Sith / Met FDC of metformien geneem, volgens die resultate was die aanvanklike Sith / Met FDC-terapie in vergelyking met metformien monoterapie voordeliger met betrekking tot glukemiese beheer, en soortgelyke aanwysers van gewigsverlies is aangeteken en 'n laer voorkoms van buikpyn en diarree. Twee vroeëre goed ontwerpte kliniese toetse by voorheen onbehandelde pasiënte met T2DM na 18 of 24 weke van Sit / Met-terapie het 'n meer duidelike verbetering in glukemiese beheer getoon as in die geval van monoterapie met 'n middel en / of placebo. En hierdie positiewe effek het voortgeduur gedurende die behandelingstydperk, wat tot 2 jaar geduur het. Gegewe die inleidingsperiode wat deur die studie-ontwerp vereis word, kan die beter Sieve / Met-FDC-effek wat in die huidige studie aangeteken is, gedeeltelik die feit weerspieël dat baie pasiënte nog nie voorheen behandeling ontvang het nie.
In die glimepiriedgroep is 'n hoër voorkoms van hipoglisemie waargeneem in vergelyking met die Sit / Met FDC-groep (20,1 en 5,5%). Aangesien die maksimum of finale dosis van meer as 46% van die pasiënte 1 mg was, en slegs ongeveer 17% van die pasiënte 6 mg as die maksimum of totale dosis ontvang het, word hierdie resultate waarskynlik verwag. Alhoewel die huidige studie titrasie van 'n dosis glimepiried volgens die oordeel van die dokters moontlik gemaak het, moet daar op gelet word dat die dokters weens die dubbelblinde aard van die studie nie inligting oor die spesifieke behandeling het nie. Dus weerspieël hierdie studie die werklike praktyk om die dosis glimepiried passief te verhoog. 'N Interessante feit is dat 'n hoër voorkoms van hipoglukemie in die glimepiriedgroep waar 'n relatiewe lae dosis toegedien is. Gegewe die bekommernisse wat verband hou met hipoglukemie, kan die gebruik van 'n sulfonielureum afgeleide terapie-behandeling die bereiking van die teiken glukemiese vlak vertraag. Daarbenewens is 'n dosisafhanklikheid getoon vir die hipoglukemie wat deur sulfonielureumderivate veroorsaak is, sowel as 'n omgekeerde korrelasie met die toename in BMI, wat 'n aanneemlike verklaring kan wees vir die toename in liggaamsgewig in die glimepiriedgroep in die huidige studie.
In die Sit / Met FDC-groep is 'n relatiewe lae frekwensie van staking van terapie waargeneem in vergelyking met die glimepiriedgroep (17,7 en 25,5%). Alhoewel die uitvalsyfer in beide groepe hoog lyk, gesien die duur van die studie (39 weke), is hierdie waarde binne 'n aanvaarbare reeks.
Die voorgestelde studie het die effektiwiteit en veiligheid van monoterapie (glimepiride) en tweekomponentterapie (Sit / Met FDC) vergelyk. 'N Aantal vorige studies het ook monoterapie en kombinasieterapie 31, 36, 37 vergelyk
enige twyfel oor die keuse van medisyne in hierdie studie is ongegrond. Daarbenewens is die feit dat glimepiride tans 'n eerste-middel middel by pasiënte met tipe 2-diabetes in Korea, 'n bykomende rede vir die gebruik daarvan in die vergelykingsgroep in die huidige studie.
Alhoewel 628 pasiënte vir hierdie studie gekeur is, is slegs 292 mense na enige terapeutiese groep gerandomiseer.Die meeste gevalle waar pasiënte nie by die keurresultate opgeneem is nie, was te wyte aan baie lae of hoë HbA1c-waardes, lae kreatinienopruiming en ander parameters wat nie aan die seleksiekriteria voldoen nie. Die eienskappe van baie pasiënte het tydens die inleidingsperiode nie aan die gespesifiseerde kriteria voldoen nie as gevolg van lae vlakke van HbA1c, wat waarskynlik te wyte was aan veranderinge in die lewenstyl van pasiënte gedurende die 6-week-inleidingsperiode. Dit bevestig die voordelige effek van 'n gesonde leefstyl op die verloop van diabetes. Boonop kan, soos voorheen bespreek, titrasie met toenemende dosisse glimepiried onvoldoende wees, wat ook die resultate van die studie kan beïnvloed.
Ten slotte moet daarop gelet word dat die gebruik van kombinasieterapie in die vroeë stadiums van behandeling aan die moderne standaarde van mediese sorg vir diabetes voldoen. Die huidige studie is die eerste om die veiligheid en effektiwiteit van Sit / Met in 'n vaste kombinasie te evalueer in vergelyking met glimepiride in Koreaanse pasiënte met T2DM as aanvanklike terapie. Die resultate van hierdie studie dui daarop dat Sit / Met FDC 'n goeie aanvanklike behandelingsopsie kan wees vir pasiënte met tipe 2-diabetes in vergelyking met glimiramide monoterapie. Verdere studies is nodig om die langtermyneffekte van Sit / Met FDC en die effek van hierdie kombinasie op die eindpunte van die kardiovaskulêre stelsel, sowel as die sterfte onder pasiënte met T2DM, te evalueer.
■ Die kombinasie van Sit / Met as die aanvanklike terapie het 30 weke na die aanvang 'n meer duidelike verbetering in die vas van glukemiese beheer en vastende plasmaglukose (GPN) gelewer, vergeleke met glimepiride. Daarbenewens, met die gebruik van Sit / Met, is 'n geringe afname in liggaamsgewig en minder uitgesproke hipoglukemie waargeneem in vergelyking met glimepiriedterapie.
■ Die huidige studie beoordeel vir die eerste keer die veiligheid en effektiwiteit van Sit / Met in 'n vaste stof
kombinasie in vergelyking met glimepiride in Koreaanse pasiënte met tipe 2-diabetes mellitus (T2DM) as aanvanklike terapie.
■ Statisties beduidende resultate van die studie: die kombinasie van Sit / Met as die aanvanklike terapie het 'n meer duidelike verbetering in die vlakke van HbA1c en GPN 30 weke na die begin vergeleke met glimepiride. Glimepiride-terapie het tot 'n toename in liggaamsgewig gelei, terwyl die gebruik van Sit / Met 'n geringe afname en minder uitgesproke hipoglukemie getoon het.
■ Wat hierdie studie bied: Hierdie studie beoordeel eerstens die veiligheid en doeltreffendheid van die Sit / Met-kombinasie in vergelyking met glimepiried-monoterapie as 'n aanvanklike behandeling by Koreaanse pasiënte met tipe 2-diabetes.
Hierdie studie is befonds deur MSD International GmbH, 'n filiaal van Merck & Co., Inc. (Kenilworth, New Jersey, VSA). Die borg het deelgeneem aan die ontwerp van die navorsing, die versameling, hersiening en ontleding van data, sowel as aan die skryf van die verslag. Tejas Tirodkar (Cactus Communications, Mumbai, Indië) het hulp verleen met die skryf van die mediese teks. Hierdie hulp is befonds deur MSD Korea Ltd. Die skrywers bedank al die navorsers wat aan die studie deelgeneem het: Young Sik Choi (Evangeliese kliniek aan die Kosin Universiteit), Jong Ryeal Hahm (kliniek van die Gyeongsang State University), Mi Kyung Kim (Maryknoll Medical Center), Ja Young Park (St. Mary's Busan Clinic) ), Sung Rae
Cho (Fatima Clinic in Changwon), Kyung Mook Choi (Guro Clinic aan die Universiteit van Korea), Dae Jung Kim (Aju University Clinic), Ki Young Lee (Gil Medical Center by Gachon University), Chong Hwa Kim (Ilsan Clinic, Staatsgesondheidsversekeringsdiens) ), Dong Jun Kim (Ilsan Peck-kliniek, Universiteit van Inje), Choon Hee Chung (aparte Christelike kliniek vir Wongju), Ji Oh Mok (Phocong-hospitaal aan die Sun-Chun-hyang-universiteit) en Sung Hee Choi (Bundang-kliniek, State University of Seoul).
SJL is 'n werknemer van MSD Korea Ltd, al die ander outeurs het geen belangebotsings wat bekend gemaak moet word nie.
Hierdie studie is geregistreer in die Cli-nicalTrials.gov databasis (ID: NCT00993187).
LEIDENDE BESTUURSINLIGTING
Kim In Joo, Afdeling Endokrinologie en Metabolisme, Afdeling Terapie, Busan State University Hospital, Suid-Korea E-pos: [email protected]
1. American Diabetes Association. Diagnose en klassifikasie van diabetes mellitus. Diabetesversorging. 2014, 37 (SuppL 1): S81-90.
2. Miller B.R., Nguyen H., Hu C.J., Lin C., Nguyen Q.T. Nuwe en opkomende medisyne en teikens vir tipe 2-diabetes: hersien die getuienis. Is voordele vir geneesmiddels by die gesondheid. 2014, 7: 452-63.
3. Wêreldgesondheidsorganisasie. Feiteblad vir diabetes. 2015. URL: http: // www.who.int/mediacentre/factsheets/fs312/en/ (datum van toegang 1 Februarie 2016).
4. Jeon J.Y., Ko S.H., Kwon H.S., et al. Voorkoms van diabetes en prediabetes volgens vastende plasmaglukose en HbA1c. Diabetes Metab J. 2013, 37: 349-57.
5. Cade W.T. Diabetes-verwante mikrovaskulêre en makrovaskulêre siektes in die fisiese terapie-omgewing. Fisioterapie. 2008, 88: 1322-35.
6. Stratton I.M. Adler A.I., Neil H.A.W., et al. Assosiasie van glykemie met makrovaskulêre en mikrovaskulêre komplikasies van tipe 2-diabetes (UKPDS 35): voornemende waarnemingsstudie. BMJ. 2000, 321: 405-12.
7. Aksie om kardiovaskulêre risiko te beheer in die Diabetesstudiegroep, Gerstein H.C., Miller M.E., et al. Effekte van intensiewe glukoseverlaging in tipe 2-diabetes. N Engl J Med. 2008, 358: 2545-59.
8. ADVANCE Collaborative Group, Patel A., MacMahon S. et al. Intensiewe beheer van bloedglukose en vaskulêre uitkomste by pasiënte met tipe 2-diabetes. N Engl J Med. 2008, 358: 2560-72.
9. Duckworth W., Abraira C., Moritz T., et al. Glukosebeheer en vaskulêre komplikasies by veterane met tipe 2-diabetes. N Engl J Med. 2009, 360: 129-39.
10. UK UK Prospective Diabetes Study (UKPDS) Group. Intensiewe beheer van bloedglukose met sulfonylurea of insulien in vergelyking met konvensionele behandeling en die risiko van komplikasies by pasiënte met tipe 2-diabetes (UKPDS 33). Lancet. 1998, 352: 837-53.
11. Holman R.R., Paul S.K., Bethel M.A., Matthews D.R., et al. 10-jarige opvolg van intensiewe glukosebeheer by tipe 2-diabetes. N Engl J Med. 2008, 359: 1577-89.
12. Riddle M.C., Yuen K.C. Herwaarderingsdoelwitte van insulinterapie: perspektiewe van groot kliniese proewe. Endocrinol Metab Clin North Am. 2012, 41: 41-56.
13. AACE omvattende algoritme vir diabetesbestuur. Taakmag op die nuwe omvattende diabetes-algoritme. Endocr Praktyk. 2013, 19 (Suppl. 2): 1-48.
14. Derosa G., Maffioli P. Pasiëntoorwegings en kliniese nut van 'n vaste dosis-kombinasie van saksagliptien / metformien in die behandeling van tipe 2-diabetes. Diabetes Metab Syndr Obes. 2011, 4: 263-71.
15. American Diabetes Association. Benaderings tot glukemiese behandeling. Diabetesversorging. 2015, 38 (Suppl. 1): S41-88.
16. Defronzo R.A. Banting-lesing. Vanaf die triumvirateto die onheilspellende octet: 'n nuwe paradigma vir die behandeling van tipe 2-diabetes mellitus. Diabetes. 2009, 58: 773-95.
17. Suk J.H., Lee C.W., Son S.P., et al. Huidige status van voorskrif by tipe 2-diabetiese pasiënte van algemene hospitale in Busan. Diabetes Metab J. 2014, 38: 230-9.
18. Davis S.N. Die rol van glimepiride in die effektiewe hantering van tipe 2-diabetes. Komplikasies van diabetes. 2004, 18: 367-76.
19. Korytkowski M.T. Sulfonylurea behandeling van tipe 2-diabetes mellitus: fokus op glimepiride. Farmakoterapie. 2004, 24: 606-20.
20. Currie C. J., Poole C. D., Evans M., Peters J. R., et al. Mortaliteit en ander belangrike uitkomste wat verband hou met suikersiekte met insulien en ander
anti-hiperglikemiese behandelings by tipe 2-diabetes. J Clin Endocrinol Metab. 2013, 98: 668-77.
21. Morgan C. L., Mukherjee J., Jenkins-Jones S., Holden S. E., et al. Assosiasie tussen eerste-lyn monoterapie met sulfonylureum teenoor metformien en die risiko van sterftes as gevolg van kardiovaskulêre gebeure: 'n retrospektiewe, waarnemende studie. Diabetes Obes Metab. 2014, 16: 957-62.
22. Genuth S. Moet sulfonielureum 'n aanvaarbare eerste toevoeging tot metformienterapie by pasiënte met tipe 2-diabetes bly? Nee, dit is tyd om aan te gaan! Diabetesversorging. 2015, 38: 170-5.
23. Plosker G.L. Sitagliptin: 'n Oorsig van die gebruik daarvan by pasiënte met tipe 2-diabetes mellitus. Dwelms. 2014, 74: 223-42.
24. Herman G.A., Bergman A., Stevens C., et al. Effek van orale dosisse sitagliptien, 'n dipeptidylpeptidase-4-remmer, op incretien- en plasmaglukosevlakke na 'n mondelinge glukosetoleransie toets by pasiënte met tipe 2-diabetes. J Clin Endocrinol Metab. 2006, 91: 4612-9.
25. Goldstein B.J., Feinglos M.N., Lunceford J.K. Johnson J., et al., Sitagliptin 036 Studiegroep. Effek van aanvanklike kombinasieterapie met sitagliptien, 'n dipeptidylpeptidase-4-remmer, en metformien op glukemiese beheer by pasiënte met tipe 2-diabetes. Diabetesversorging. 2007, 30: 1979-87.
26. Charbonnel B., Karasik A., Liu J., Wu M., et al., Sitagliptin Study 020 Group. Effektiwiteit en veiligheid van die dipeptidylpeptidase-4-remmer sitagliptien word bygevoeg tot voortgesette metformienterapie by pasiënte met tipe 2-diabetes wat onvoldoende beheer word met metformien alleen. Diabetesversorging. 2006, 29: 2638-43.
27. Miettinen O., Nurminen M. Vergelykende analise van twee tempo's. Stat Med. 1985, 4: 213-26.
28. Chwieduk C.M. Sitagliptien / metformien-kombinasie met vaste dosis: In pasiënte met tipe 2-diabetes mellitus. Dwelms. 2011, 71: 349-61.
29. Lee Y.K., Song S.O., Kim K.J., et al. Glykemiese effektiwiteit van metformien-gebaseerde tweeledige-kombinasie-behandelings met sulfonielureum, pioglitazon of DPP4-remmer by pasiënte met dwelm-naïewe Koreaanse tipe 2-diabeet. Diabetes Metab J. 2013, 37: 465-74.
30. Chung H.S., Lee M.K. Effektiwiteit van sitagliptien wanneer dit bygevoeg word tot deurlopende terapie by Koreaanse persone met tipe 2-diabetes mellitus. Diabetes Metab J. 2011, 35: 411-7.
31. Kim H.S., Kim D.M., Cha B.S., et al. Doeltreffendheid van glamepiried / metformien-kombinasie met vaste dosis teenoor metformienopname in tipe 2-diabetiese pasiënte wat onvoldoende beheer word met 'n lae-dosis metformien monoterapie: 'n gerandomiseerde, oop etiket, parallelle groep, multisenterstudie in Korea. J Diabetes Ondersoek. 2014, 5: 701-8.
32. Derosa G., Salvadeo S.A. Pioglitazon en metformien-vaste dosis-kombinasie in tipe 2-diabetes mellitus: 'n bewysgebaseerde oorsig van die plek in terapie. Kernontsteking. 2008, 2: 189-98.
33. Vanderpoel D.R., Hussein M.A., Watson-Heidari T., Perry A. Voldoening aan 'n vaste-dosis-kombinasie van rosiglitazonmaleaat / metformin-hidrochloried by persone met tipe 2-diabetes mellitus: 'n retrospektiewe databasisontleding. Clin Ther. 2004, 26: 2066-75.
34. Bain S.C. Behandeling van tipe 2-diabetes mellitus met oraal toegediende middels: vooruitgang in kombinasieterapie. Endocr Praktyk. 2009, 15: 750-62.
35. Perez-Monteverde A., Seck T., Xu L., et al. Doeltreffendheid en veiligheid van sitagliptien en die vaste dosis-kombinasie van sitagliptien en metformien vs. pioglitazoon by naïewe medisyne pasiënte met tipe 2-diabetes. Int J Clin Praktyk. 2011, 65: 930-8.
Fyn-tuning-tipe 2-diabetes mellitus-terapie
| í Amaryl '1 * 1 I Amaryl' j Amaryl ■ Amaryl '
II 1 tmr-lm ■ 'I Ts 1 IM HTM', p. “Jare, n!
I 1 iHNOF '^ yifiÖ ^ O
Meer as 15 jaar in Rusland1
Dubbele werkingsmeganisme: stimulasie van insulienafskeiding en 'n afname in insulienweerstandigheid2
Vermindering van glukemie in kombinasie met 'n lae risiko vir hipoglukemie met glimepiried in die werklike kliniese praktyk in Rusland 3-5
Gerieflike toediening: 1 tablet 1 keer per dag2
Verskeie dosisse vir maklike titrasie2
Ekonomiese vorm van vrystelling - 90 tablette in een pakket6 *
Kort instruksies vir mediese praktyke
D van die middel AMARIL®
Handelsnaam van die preparaat: Amaril®. Internasionale nie-eienaardige naam: glimepiride. Dosisvorm en samestelling: tablette. Amaryl® 1.2.3.4 mg: 1 tablet bevat onderskeidelik 1.2.3.4 mg glimepiried. Farmakoterapeutiese groep: hipoglisemiese middel vir orale toediening van die III-generasie sulfonylureumgroep. Indikasies vir gebruik: tipe 2-diabetes mellitus (in monoterapie of as deel van kombinasie-behandeling met metformien of insulien). Dosis en toediening: Amaril® tablette word heel geneem sonder om te kou, en baie vloeistof ™ gedrink (ongeveer 0,5 koppies). Die aanvanklike dosis is 1 mg glimepiried 1 keer per dag. Daar word aanbeveel dat die dosisverhoging uitgevoer word onder gereelde monitering van die bloedglukosekonsentrasie en in ooreenstemming met die volgende dosisverhogingstap: 1 mg-2 mg-Zmg-4 mg-6 mg-8 mg met tussenposes van 1-2 weke. Dit word geneem voor 'n volledige ontbyt of hoofmaaltyd. Kontraïndikasies: tipe 1-diabetes mellitus, diabetiese ketoasidose, diabetiese precoma en koma, hipersensitiwiteit vir glimepiride of vir enige van die hulpkomponente van die middel, vir ander sulfonylurea of sulfonamiede, swangerskap en laktasie, ernstige lewerfunksie, ernstige nierfunksie, kinders ouderdom (gebrek aan kliniese gegewens oor gebruik), seldsame oorerflike siektes (galaktose-intoleransie, laktase-tekort of glukose-galaktose malabsor btsiya). Met omsigtigheid: in die eerste weke van die behandeling, in die teenwoordigheid van risikofaktore vir die ontwikkeling van hipoglukemie (sien die volledige instruksies vir die medisyne-gebruik van die middel), vir tussentydse siektes, veranderinge in die lewenstyl van pasiënte, glukose-6-fosfaat dehidrogenase-tekort, en wanabsorpsie in die maag. obstruksie, dermparese).Spesiale instruksies: in die eerste weke van die behandeling kan die risiko van hipoglukemie toeneem - noukeurige monitering van glukemie word benodig. In die geval van spesiale kliniese stresvolle toestande (trauma, chirurgiese ingrepe, infeksies met koorsige temperatuur), kan 'n tydelike oorgang na insulienterapie nodig wees. Interaksie met ander geneesmiddels: glimepiride word gemetaboliseer deur sitochroom P4502C9 (CYP2C9), wat in ag geneem moet word wanneer dit gelyktydig met induseerders (bv. Rifampisien) of remmers (bv. Flukonasool) CYP2C9 gebruik word. Raadpleeg die volledige aanwysings vir die mediese gebruik van die middel vir interaksie met ander medisyne. Newe-effek: hipoglukemie. In seldsame gevalle: naarheid, braking, ongemak in die epigastrium, diarree, 'n kortstondige toename in die aktiwiteit van lewerensieme en / of cholestase, hepatitis, kortstondige gesiggestremdheid as gevolg van 'n verandering in bloedglukosekonsentrasie, trombositopenie, leukopenie, hemolitiese anemie, eritrocytopenia, granulocytopenia , agranulocytosis, pancytopenia, pruritus, urticaria, veluitslag, allergiese vaskulitis, fotosensitiwiteit. Oordosis: akute oordosis, sowel as langdurige behandeling met te hoë dosisse glimepiried, kan lei tot ernstige, lewensgevaarlike hipoglukemie. Sodra 'n oordosis opgemerk word, moet u u dokter onmiddellik in kennis stel. Hipoglukemie kan byna altyd vinnig gestop word deur die onmiddellike inname van koolhidrate. ATX-kode: A10BB12. Vervaldatum: 3 jaar. Voor die afspraak moet u die instruksies vir die gebruik van die dwelm lees
1. Registrasiesertifikaat van die dwelm Amaril® vir medies gebruik П П N015530 / 01. 2. Instruksies vir die mediese gebruik van Amaril®, per, nommer P N015530 / 01-131216.3. Ametov A.C. met eoavt. Moontlikhede om glimepiried te gebruik om suikerverlagende terapie te begin. Resultate van 'n Amaril-MONO-waarnemingstudie. Diabetes mellitus, 2013: No. 3. 4. Glinkina I.V. et al., effektiwiteit en veiligheid van die gratis kombinasie van glimepiride en metformien by pasiënte met tipe 2-diabetes mellitus in die werklike kliniese praktyk: 'n waarnemingsprogram // Effektiewe farmakoterapie. Endokrinologie 2/2012: 16-20.5. Zaitseva N.V. et al., <Kombinasieterapie met glimepiride en metformien in pasiënte met tipe 2-diabetes. Die resultate van die Russiese waarnemingsstudie // Farmateka. - 2014. - No. 16.6. www.apteka.ru, laaste toegang tot die webwerf - 07/06/2017. "Die koste van een tablet in 'n verpakking nr. 90 is 25% laer as die koste van een tablet in 'n verpakking nr. 30 vir vergelykbare dosisse. # Die klassieke benadering tot die behandeling van tipe 2-diabetes mellitus: stimulering van insulienafskeiding en> vermindering van insulienweerstandigheid. Inligting is bedoel vir gesondheidswerkers
Verteenwoordiging van die lyk van Sanofi-aventis JSC (Frankryk) 125009, Moskou, ul. Tverskaya, d. 22. Telefoon: (495) 721-14-00, faks: (495) 721-14-11, www.sanofi.ru.SARU.GLI.17.06.0953
36. Reasner C., Olansky L., Seck T. L., et al. Die effek van aanvanklike terapie met die vaste dosis-kombinasie van sitagliptien en metformien in vergelyking met metformien monoterapie by pasiënte met tipe 2-diabetes mellitus. Diabetes Obes Metab. 2011, 13: 644-52.
37. Wainstein J., Katz L., Engel S.S., et al. Aanvanklike terapie met die vaste dosis-kombinasie van sitagliptien en metformien lei tot 'n groter verbetering in glukemiese beheer in vergelyking met pioglitazon.
monoterapie by pasiënte met tipe 2-diabetes. Diabetes Obes Metab. 2012, 14: 409-18.
Farmakologie
Metformin + sitagliptin is 'n kombinasie van twee aktiewe stowwe (DV) met 'n komplementêre (komplementêre) werkingsmeganisme - sitagliptien, 'n DPP-4-remmer, en metformien, 'n verteenwoordiger van die biguaniedklas. Dit word gebruik om glukemiese beheer te verbeter by pasiënte met tipe 2-diabetes.
As oraal toegedien word, is sitagliptin 'n aktiewe hoogs selektiewe DPP-4-remmer, bedoel vir die behandeling van tipe 2-diabetes mellitus. Die farmakologiese effekte van die klas medisyne - DPP-4-remmers word bemiddel deur die aktivering van inkretiene. Deur DPP-4 te inhibeer, verhoog sitagliptien die konsentrasie van twee bekende aktiewe hormone van die inkretienfamilie: GLP-1 en HIP.Die inkretiene vorm deel van die interne fisiologiese stelsel vir die regulering van glukose-homeostase. By normale of verhoogde bloedglukosekonsentrasies verhoog GLP-1 en GUI's die sintese en afskeiding van insulien deur die beta-selle van die pankreas. GLP-1 onderdruk ook die afskeiding van glukagon deur alfa-selle in die pankreas en verminder sodoende die sintese van glukose in die lewer. Hierdie werkingsmeganisme verskil van die werking van sulfonielureumderivate, wat die vrystelling van insulien stimuleer selfs by lae bloedglukosekonsentrasies, wat belaai is met die ontwikkeling van sulfoniel-geïnduseerde hipoglykemie, nie net by pasiënte met tipe 2-diabetes mellitus nie, maar ook by gesonde individue. As 'n baie selektiewe en effektiewe remmer van die DPP-4-ensiem, belemmer sitagliptien in terapeutiese konsentrasies nie die aktiwiteit van die verwante ensieme DPP-8 of DPP-9 nie. Sitagliptien verskil in chemiese struktuur en farmakologiese werking van analoë van GLP-1, insulien, sulfonylureumderivate of meglitiniede, biguanides, gamma-reseptoragoniste wat geaktiveer word deur peroxis proliferator (PPARγ), alfa-glukosidase-remmers en amylien-analoë.
Metformien is 'n hipoglisemiese middel wat glukosetoleransie verhoog by pasiënte met tipe 2-diabetes, wat die basale en postprandiale glukosekonsentrasie verlaag. Die farmakologiese werkingsmeganismes daarvan verskil van die meganismes van werking van orale hipoglisemiese middels in ander klasse.
Metformien verminder die sintese van glukose in die lewer, die opname van glukose in die ingewande en verhoog insulien sensitiwiteit deur die perifere opname en die gebruik van glukose te verhoog. Anders as sulfonylureumderivate, veroorsaak metformien nie hipoglukemie by pasiënte met tipe 2-diabetes mellitus of by gesonde mense nie (met die uitsondering van sommige omstandighede, sien "Beperkings op die gebruik", metformien) en veroorsaak nie hiperinsulinemie nie. Tydens behandeling met metformien verander die insulienafskeiding nie, terwyl die konsentrasie van insulien op 'n leë maag en die daaglikse waarde van die plasmakonsentrasie van insulien kan daal.
Die orale toediening van 'n enkele dosis sitagliptien aan pasiënte met tipe 2-diabetes mellitus lei tot 'n onderdrukking van die aktiwiteit van die DPP-4-ensiem gedurende 24 uur, wat gepaard gaan met 'n twee tot drie-voudige toename in die konsentrasie van die sirkulerende aktiewe GLP-1 en HIP, 'n toename in die plasmakonsentrasie van insulien en C-peptied, 'n afname in die konsentrasie van glukagon en vinnige plasmaglukosekonsentrasie, sowel as 'n afname in die amplitude van glukemiese skommelinge na glukose of voedselbelading.
Die toediening van sitagliptien in 'n daaglikse dosis van 100 mg vir 4-6 maande het die funksie van pankreas beta-selle in pasiënte met tipe 2-diabetes mellitus aansienlik verbeter, soos blyk uit die ooreenstemmende veranderinge in merkers soos HOMA-β (assessering van homeostase in model-β), die verhouding proinsulien / insulien, evaluering van die reaksie van beta-selle in die pankreas volgens die paneel van herhaalde toetse vir voedseltoleransie. Volgens kliniese studies van die II- en III-fases, was die effektiwiteit van glukemiese beheer van sitagliptien in die behandeling van 50 mg 2 keer per dag vergelykbaar met die doeltreffendheid van die 100 mg-skema een keer per dag.
In 'n gerandomiseerde, placebo-gekontroleerde, dubbelblinde, dubbele-gesimuleerde 4-periodes deursnitstudie by gesonde vrywilligers, is die effekte van sitagliptien in kombinasie met metformien, of slegs sitagliptien, of slegs metformien, of placebo op veranderinge in plasmakonsentrasies van aktiewe en totale GLP-1 en glukose na toediening bestudeer. kos. Die geweegde gemiddelde waardes van die konsentrasie van aktiewe GLP-1 4 uur na 'n maaltyd het ongeveer 2 keer gestyg nadat slegs sitagliptien of slegs metformien geneem is, vergeleke met placebo. Die gekombineerde toediening van sitagliptien en metformien het 'n opsomming van die effek verseker met 'n viervoudige toename in die konsentrasie van aktiewe GLP-1 in vergelyking met die dinamika in die placebogroep.
Die ontvangs van sitagliptien alleen gaan gepaard met 'n toename in die konsentrasie van slegs aktiewe GLP-1 as gevolg van die remming van die DPP-4-ensiem, terwyl die toediening van metformien alleen gepaard gaan met 'n simmetriese toename in die konsentrasie van totale en aktiewe GLP-1. Die data wat verkry is, weerspieël verskillende meganismes onderliggend aan die toename in die konsentrasie van aktiewe GLP-1 na die inname van hierdie twee middels. Die resultate van die studie het ook getoon dat dit sitagliptien en nie metformien was nie, wat die konsentrasie van aktiewe GLP-1 verhoog het.
In studies by gesonde vrywilligers, het die neem van sitagliptien nie gepaard gegaan met 'n afname in glukosekonsentrasie nie en dit het ook nie hipoglisemie veroorsaak nie, wat die glukose-afhanklike aard van die insulienotropiese effek en die onderdrukking van glukagon-sintese bevestig.
In 'n gerandomiseerde, placebo-gekontroleerde studie waarby pasiënte met arteriële hipertensie betrokke was, is die gekombineerde gebruik van anti-hipertensiewe medisyne (een of meer van die lys: ACE-remmers, ARA II, BKK, beta-blokkers, diuretika) met sitagliptien, algemeen deur pasiënte verdra. In hierdie kategorie pasiënte het sitagliptien 'n effense hipotensiewe effek getoon: in 'n daaglikse dosis van 100 mg het sitagliptin die gemiddelde daaglikse ambulante waarde van SBP met 2 mm Hg verlaag. in vergelyking met die placebo groep. By pasiënte met normale bloeddruk is geen hipotensiewe effek waargeneem nie.
Effek op elektrofisiologie van die hart
In 'n gerandomiseerde, placebo-gekontroleerde oorgangstudie by gesonde vrywilligers, is sitagliptien een keer gebruik in 'n dosis van 100 of 800 mg (8 keer meer as die aanbevole dosis) of placebo. Na die aanbevole terapeutiese dosis van enige effek van die geneesmiddel op die duur van die QT-interval, soos op die tydstip van plasma CMax en tydens ander studie, is daar nie op ander punte van verifiëring waargeneem nie. Na inname van 800 mg was die maksimum toename in die placebo-aangepaste gemiddelde verandering in die duur van die QT-interval, vergeleke met die aanvanklike waarde 3 uur na inname van die middel, 8 ms. 'N Soortgelyke toename is as klinies onbeduidend beoordeel. Nadat u 800 mg geneem het, is die plasma C-waardeMax Sitagliptien was ongeveer 11 keer groter as die ooreenstemmende waarde na die neem van 'n terapeutiese dosis van 100 mg.
Die resultate van 'n bioekwivalensie-studie by gesonde vrywilligers het getoon dat kombinasie tablette (metformien + sitagliptien) 500/50 mg en 1000/50 mg bioekwivalent is aan die afsonderlike toediening van die toepaslike dosisse sitagliptien en metformien.
Gegewe die bewese bioekwivalensie van die tablette met die laagste en hoogste dosisse metformien, is tablette met 'n intermediêre dosis metformien (metformin + sitagliptin) 850/50 mg ook bioekwivalensie gegee, mits die vaste dosis-kombinasie in die tablet gekombineer is.
Sitagliptin. Die absolute biobeskikbaarheid van sitagliptien is ongeveer 87%. Die gebruik van sitagliptien op dieselfde tyd as 'n vetterige maaltyd beïnvloed nie die farmakokinetika van die kombinasie nie.
Metformin. Die absolute biobeskikbaarheid van metformien as dit op 'n leë maag geneem word in 'n dosis van 500 mg is 50-60%. Die resultate van studies van 'n enkele dosis metformien in dosisse van 500 tot 1500 mg en van 850 tot 2550 mg dui op 'n skending van die dosisproportionaliteit met 'n toenemende dosis, wat waarskynliker is as gevolg van verminderde opname eerder as versnelde uitskeiding. Gelyktydige gebruik met voedsel verlaag die tempo en hoeveelheid geabsorbeerde metformien, wat blyk uit 'n afname in plasma CMax met ongeveer 40%, 'n afname in AUC van ongeveer 25%, en 'n vertraging van 35 minute om C te bereikMax na 'n enkele dosis metformien in 'n dosis van 850 mg gelyktydig met voedsel in vergelyking met die waardes van die ooreenstemmende parameters, nadat 'n soortgelyke dosis van die middel op 'n leë maag geneem is. Die kliniese belang van die verlaging van die farmakokinetiese parameters is nie vasgestel nie.
Sitagliptin. Medium Vss Na 'n enkele iv-inspuiting is 100 mg sitagliptien by gesonde vrywilligers ongeveer 198 liter. Die fraksie van sitagliptien wat omkeerbaar is aan plasmaproteïene is relatief klein (38%).
Metformin. Vd metformien na 'n enkele orale dosis van 850 mg gemiddeld (654 ± 358) l. Metformien bind slegs tot 'n baie klein mate aan plasmaproteïene. Metformien word gedeeltelik en tydelik in rooibloedselle versprei. Wanneer metformien in aanbevole dosisse en modusse gebruik word, plasma Css (gewoonlik CMax het nie 5 μg / ml oorskry nie, selfs nie na die neem van die maksimum dosisse nie.
Sitagliptin. Ongeveer 79% van sitagliptien word onveranderd deur die niere uitgeskei, metaboliese transformasie is minimaal.
Nadat 14 C-gemerkte sitagliptien oraal toegedien is, is ongeveer 16% van die toegediende radioaktiwiteit as sitagliptienmetaboliete uitgeskei. Spoorkonsentrasies van 6 sitagliptienmetaboliete is geïdentifiseer wat nie tot die plasma DPP-4-remmende werking van sitagliptien bygedra het nie. In studies in vitro isoënsieme van die sitochrome stelsel CYP3A4 en CYP2C8 word geïdentifiseer as die belangrikste wat betrokke is by die beperkte metabolisme van sitagliptien.
Metformin. Na 'n enkele IV-toediening aan metformien gesonde vrywilligers, is byna die hele dosis wat toegedien is, onveranderd deur die niere uitgeskei. Metaboliese veranderinge in die lewer en uitskeiding met gal kom nie voor nie.
Sitagliptin. Nadat gesonde vrywilligers 14 C-gemerkte sitagliptien ingeneem het, is byna al die ingevoerde radioaktiwiteit binne 'n week uit die liggaam verwyder, insluitend 13% deur die ingewande en 87% deur die niere. Gemiddeld T1/2 sitagliptien met orale toediening van 100 mg is ongeveer 12,4 uur, nieropruiming is ongeveer 350 ml / min.
Uitskeiding van sitagliptien word hoofsaaklik uitgevoer deur nieruitskeiding deur die meganisme van aktiewe tubulêre sekresie. Sitagliptin is 'n substraat van die vervoerder van organiese menslike anione van die derde soort (h hAT-3), wat betrokke is by die uitskakeling van sitagliptien deur die niere. Die kliniese belang van die betrokkenheid van hOAT-3 by die vervoer van sitagliptien is nie vasgestel nie. P-gp kan betrokke wees by die eliminasie van sitagliptien (as substraat) nier, maar die P-gp-remmer siklosporien verminder egter nie die renale klaring van sitagliptien nie.
Metformin. Nieropruiming van metformien oorskry kreatinienopruiming met 3,5 keer, wat 'n aktiewe nierafskeiding as die belangrikste uitskeidingsroete aandui. Na die inname van metformien word ongeveer 90% van die geabsorbeerde middel gedurende die eerste 24 uur deur die niere uitgeskei by 'n plasma T1/2 ongeveer 6,2 uur, in die bloed word hierdie waarde uitgebrei tot 17,6 uur, wat die moontlike deelname van rooibloedselle as 'n potensiële verspreidingsruimte aandui.
Farmakokinetika in individuele pasiëntgroepe
Tipe 2-diabetes pasiënte
Sitagliptin. Die farmakokinetika van sitagliptien by pasiënte met tipe 2-diabetes is soortgelyk aan die farmakokinetika by gesonde individue.
Metformin. Met die behoue nierfunksie is die farmakokinetiese parameters na 'n enkele en herhaalde toediening van metformien by pasiënte met tipe 2-diabetes mellitus en gesonde individue dieselfde. Ophoop die geneesmiddel nie wanneer terapeutiese dosisse geneem word nie.
Die kombinasie van metformien + sitagliptien moet nie aan pasiënte met nierversaking voorgeskryf word nie (sien "Kontraïndikasies").
Sitagliptin. In pasiënte met matige nierversaking, is 'n ongeveer tweevoudige toename in die plasma-AUC van sitagliptien waargeneem, en by pasiënte met ernstige en terminale stadiums (op hemodialise), was die toename in AUC viervoudig vergeleke met die kontrolewaardes by gesonde individue.
Metformin. In pasiënte met verminderde nierfunksie (kreatinienopruiming) T1/2 verleng, en die renale klaring neem af in verhouding tot 'n afname in kreatinienopruiming.
Sitagliptin. By pasiënte met matige leverinsufficiëntie (7–9 punte op die Child-Pugh-skaal) is die gemiddelde waardes van AUC en CMax sitagliptien na 'n enkele dosis van 100 mg verhoog met onderskeidelik ongeveer 21 en 13%, vergeleke met gesonde individue. Hierdie verskil is nie klinies beduidend nie. Daar is geen kliniese gegewens oor die gebruik van sitagliptien by pasiënte met ernstige leverinsufficiëntie nie (meer as 9 punte op die Child-Pugh-skaal). Op grond van die oorwegend nieruitskeidingsroete, word beduidende veranderinge in die farmakokinetika van sitagliptien egter nie voorspel nie.
Metformin. Ondersoek is gedoen na die farmakokinetiese parameters van metformien by pasiënte met lewerversaking.
Sitagliptin. Volgens die ontleding van die farmakokinetiese data van kliniese toetse van fase I en II, het geslag geen klinies beduidende effek op die farmakokinetiese parameters van sitagliptien gehad nie.
Metformin. Die farmakokinetiese parameters van metformien verskil nie betekenisvol in gesonde individue en pasiënte met tipe 2-diabetes mellitus op grond van geslag nie. Volgens gekontroleerde kliniese studies was die hipoglisemiese effekte van metformien by mans en vroue soortgelyk.
Sitagliptin. Volgens die populasie farmakokinetiese ontleding van data uit kliniese toetse van fase I en II, het die ouderdom van die pasiënte nie 'n klinies beduidende effek op die farmakokinetiese parameters van sitagliptien gehad nie. Die konsentrasie van sitagliptien by ouer pasiënte (65-80 jaar) was ongeveer 19% hoër as by jong pasiënte.
Metformin. Beperkte gegewens uit gekontroleerde farmakokinetiese studies van metformien by gesonde ouer persone dui daarop dat hul totale plasmaklaring verminder word, T1/2 verleng, en die waarde van CMax stygings vergeleke met jong gesonde individue. Hierdie gegewens beteken dat ouderdomsverwante veranderinge in die farmakokinetika van metformien te wyte is aan 'n afname in die uitskeiding van die nier.
Behandeling met die kombinasie van metformien + sitagliptien word nie vir bejaardes op die ouderdom van 80 jaar aangedui nie, met die uitsondering van mense wie se kreatinienopruiming aandui dat die nierfunksie nie verminder word nie (sien "Voorsorgmaatreëls", metformien).
Ondersoek is gedoen na die kombinasie van metformien + sitagliptien by kinders.
Sitagliptin. Volgens die ontleding van farmakokinetiese data uit kliniese toetse van fase I en II, het ras geen klinies beduidende effek op die farmakokinetiese parameters van sitagliptien gehad nie, insluitend verteenwoordigers van die Kaukasiese en Mongoloid-rasse, verteenwoordigers van Latyns-Amerikaanse lande en ander etniese en rassegroepe.
Metformin. Ondersoek is gedoen na die potensiële impak van ras op die farmakokinetiese parameters van metformien. Volgens gekontroleerde studies van metformien by pasiënte met tipe 2-diabetes mellitus, was die hipoglykemiese effek vergelykbaar in verteenwoordigers van die Kaukasiese, Negroid-rasse en Latyns-Amerikaanse lande.
Sitagliptin. Volgens ingewikkelde en populasie-analise van farmakokinetiese parameters uit kliniese toetse van fase I en II, het BMI nie 'n klinies beduidende effek op die farmakokinetiese parameters van sitagliptien gehad nie.
Die gebruik van stowwe Metformin + Sitagliptin
Die kombinasie van metformien + sitagliptien word aangedui as 'n beginterapie vir pasiënte met tipe 2-diabetes mellitus om glukemiese beheer te verbeter, indien die dieet en oefenprogram nie voldoende beheer toelaat nie.
Die kombinasie van metformien + sitagliptien word aangedui as 'n aanvulling op die dieet- en oefenregime om glukemiese beheer te verbeter by pasiënte met tipe 2-diabetes wat nie voldoende beheer op die agtergrond van monoterapie met metformien of sitagliptien verkry het nie, of na 'n onsuksesvolle kombinasiebehandeling met twee DV.
Die kombinasie van metformien + sitagliptien word aangedui vir pasiënte met tipe 2-diabetes mellitus om glukemiese beheer in kombinasie met sulfonielureumderivate te verbeter (drievoudige kombinasie: metformien + sitagliptin + sulfonylureumderivaat) wanneer dieet en oefenregime gekombineer word met twee van hierdie drie middels: metformien, sitagliptien of sulfonielureumderivate lei nie tot voldoende glukemiese beheer nie.
Die kombinasie van metformien + sitagliptien word aangedui vir pasiënte met tipe 2-diabetes mellitus om glukemiese beheer te verbeter in kombinasie met tiazolidinedione (PPARγ-reseptoragoniste wat deur die peroksisome proliferator geaktiveer word), wanneer die dieet en oefenregime gekombineer word met twee van hierdie drie middels: metformien, sitagliptin of tiazolidine. lei nie tot voldoende glukemiese beheer nie.
Die kombinasie van metformin + sitagliptien is aangedui vir pasiënte met tipe 2-diabetes mellitus om glukemiese beheer in kombinasie met insulien te verbeter, wanneer die dieet en oefenprogram in kombinasie met insulien nie tot voldoende glukemiese beheer lei nie.
Toepassingsbeperkings
Gebruik by bejaardes
Die kombinasie van metformien + sitagliptien. Aangesien die hoofweg vir eliminasie van sitagliptien en metformien die niere is en die uitskeidingsfunksie van die niere met die ouderdom afneem, neem die voorsorgmaatreëls toe met die voorskrif van die kombinasie van metformien + sitagliptien toe, in verhouding tot ouderdom. Bejaarde pasiënte ondergaan noukeurige dosiskeuse en monitor gereeld die nierfunksie (sien "Voorsorgmaatreëls", Nierfunksie monitering).
Sitagliptin. Volgens kliniese studies was die effektiwiteit en veiligheid van sitagliptien by bejaarde (> 65 jaar) pasiënte vergelykbaar met die effektiwiteit en veiligheid by jong pasiënte (PM, wat nie aanbeveel word vir gebruik tydens swangerskap nie).
Daar was geen eksperimentele studies oor die kombinasie van metformien + sitagliptien om die effek op voortplantingsfunksie te bepaal nie.
Sitagliptin. Sitagliptien het geen teratogenisiteit getoon tydens organogenese nie, wanneer dit oraal toegedien word aan rotte in daaglikse dosisse tot 250 mg / kg of aan konyne in dosisse tot 125 mg / kg (wat die plasma-blootstelling by mense met 32 en 22 keer oorskry, nadat die aanbevole daaglikse terapeutiese dosis van 100 mg geneem is). . 'N Geringe toename in die frekwensie van misvorming van ribbes by die nageslag is opgemerk (afwesigheid, hipoplasie, kromming) wanneer oraal toegedien word in daaglikse dosisse van 1000 mg / kg (wat die blootstelling by mense ongeveer 100 keer oorskry nadat die aanbevole daaglikse dosis van 100 mg geneem is). Daar was 'n geringe afname in liggaamsgewig by die nageslag van rotte van beide geslagte tydens borsvoeding en 'n afname in die gewigstoename aan die einde van borsvoeding by mans met orale toediening van 1000 mg / kg daaglikse dosis sitagliptien aan swanger wyfies. Eksperimentele reproduktiewe studies korreleer egter nie altyd direk met die gevolge van sitagliptien op die voortplantingsfunksie van die mens nie.
Metformin. Metformien het geen teratogenisiteit getoon wanneer dit mondelings aan rotte toegedien word in daaglikse dosisse tot 600 mg / kg nie. Dit oortref die plasma-blootstelling by mense 2 en 6 keer (onderskeidelik by rotte en konyne) nadat die maksimum aanbevole daaglikse terapeutiese dosis van 2000 mg geneem is. Die waardes van die plasmakonsentrasie in die fetus dui op gedeeltelike plasenta-oordrag.
Eksperimentele studies om die afskeiding van die komponente van die kombinasie van metformien + sitagliptien in borsmelk te bepaal, is nie uitgevoer nie. Volgens studies oor die individuele komponente word beide sitagliptien en metformien in die borsmelk van rotte afgeskei. Daar is geen data oor die afskeiding van sitagliptien in menslike borsmelk nie. Daarom moet die kombinasie van metformien + sitagliptien nie tydens laktasie voorgeskryf word nie.
Newe-effekte van Metformin + Sitagliptin
In placebo-gekontroleerde studies, is pasiënte met diabetes mellitus algemeen gekombineer met sitagliptien en metformien, maar die frekwensie van newe-effekte met gekombineerde behandeling met sitagliptien en metformien was vergelykbaar met die frekwensie by die neem van metformien in kombinasie met placebo.
Gekombineerde behandeling met sitagliptien en metformien
In 'n 24-week placebo-gekontroleerde fabrieksstudie van aanvanklike kombinasie-terapie met sitagliptien en metformien (sitagliptien 50 mg + metformin 500 of 1000 mg 2 keer per dag) in die kombinasieterapiegroep in vergelyking met metformien monoterapiegroepe (500 of 1000 mg 2 keer per dag) , sitagliptien (100 mg een keer per dag) of placebo, is die volgende newe-reaksies wat met die geneesmiddel geassosieer word, waargeneem met 'n frekwensie van ≥1% in die kombinasie-behandelingsgroep en meer gereeld as in die placebogroep: diarree (sitagliptin + metformien - 3.5%, metformien - 3,3%, sitagliptien - 0%, placebo - 1,1%), naarheid (1,6, 2,5, 0 en 0,6%), dyspepsie (1,3, 1,1, 0 en 0%), winderigheid (1.3, 0.5, 0 en 0%), braking (1.1, 0.3, 0 en 0%), hoofpyn (1.3, 1.1, 0.6 en 0%) en hipoglukemie (1,1, 0,5, 0,6 en 0%).
Sitagliptien by die huidige metformienterapie gevoeg
In 'n 24-week placebo-gekontroleerde studie, met die toevoeging van sitagliptien in 'n dosis van 100 mg / dag tot die huidige behandeling met metformien, is die enigste nadelige reaksie wat verband hou met mede-toediening waargeneem met 'n frekwensie van ≥ 1% in die behandelingsgroep met sitagliptien en meer gereeld as in die placebogroep daar was naarheid (sitagliptien + metformien - 1,1%, placebo + metformien - 0,4%).
Hipoglukemie en nadelige reaksies vanaf die spysverteringskanaal
In placebo-gekontroleerde studies van gekombineerde behandeling met sitagliptien en metformien, was die voorkoms van hipoglukemie (ongeag die oorsaaklike verband) in die kombinasieterapiegroepe vergelykbaar met die frekwensie in die behandelingsgroepe metformien gekombineer met placebo (1.3-11.6 en 2.1% onderskeidelik). Die frekwensie van gemonitorde newe-reaksies vanuit die spysverteringskanaal (ongeag die verband tussen die oorsaak en gevolg) in die gekombineerde behandelingsgroepe van sitagliptien en metformien, was vergelykbaar met die frekwensie in die metformien monoterapiegroepe: diarree (sitagliptien + metformien - 7,5%, metformien - 7,7%), naarheid (4,8, 5,5%), braking (2,1, 0,5%), buikpyn (3, 3,8%). By alle studies is newe-reaksies in die vorm van hipoglukemie aangeteken op grond van alle verslae van klinies uitgedrukte simptome van hipoglukemie, en 'n addisionele meting van bloedglukosekonsentrasie was nie nodig nie.
Gekombineerde behandeling met sitagliptien, metformien en 'n sulfonylurea-afgeleide
In 'n 24-week placebo-gekontroleerde studie met sitagliptien in 'n dosis van 100 mg / dag teen die agtergrond van die huidige gekombineerde behandeling met glimepiride in 'n dosis van ≥4 mg / dag en metformien in 'n dosis van ≥1500 mg / dag, is die volgende nadelige reaksies waargeneem met 'n frekwensie van ≥1% in die behandelingsgroep met sitagliptien en meer gereeld as in die placebogroep: hipoglykemie (sitagliptien - 13,8%, placebo - 0,9%), hardlywigheid (1,7 en 0%).
Gekombineerde behandeling met sitagliptien, metformien en PPARγ-agonis
Volgens 'n placebo-gekontroleerde studie met sitagliptien in 'n dosis van 100 mg / dag teen die agtergrond van die huidige gekombineerde behandeling met rosiglitazon en metformien, is die volgende newe-reaksies tydens die 18de week van behandeling geassosieer met die neem, waargeneem met 'n frekwensie van ≥1% in die behandelingsgroep met sitagliptien en meer gereeld dan in die placebo-groep: hoofpyn (sitagliptien - 2,4%, placebo - 0%), diarree (1,8, 1,1%), naarheid (1,2, 1,1%), hipoglukemie (1 , 2, 0%), braking (1,2, 0%). In die 54ste week van gekombineerde behandeling is die volgende newe-reaksies waargeneem geassosieer met toediening, waargeneem met 'n frekwensie van ≥ 1% in die behandelingsgroep met sitagliptien en meer gereeld as in die placebogroep: hoofpyn (sitagliptien - 2,4%, placebo - 0%) , hipoglukemie (2,4, 0%), infeksies in die boonste lugweë (1,8, 0%), naarheid (1,2, 1,1%), hoes (1,2, 0%), swaminfeksies van die vel ( 1,2, 0%), perifere edeem (1,2, 0%), braking (1,2, 0%).
Gekombineerde behandeling met sitagliptien, metformien en insulien
In 'n 24-week, placebo-gekontroleerde studie met sitagliptien in 'n dosis van 100 mg / dag teen die agtergrond van die huidige gekombineerde behandeling met metformien in 'n dosis van ≥1500 mg / dag en 'n konstante dosis insulien, die enigste nadelige reaksie wat verband hou met die inname van die middel en waargeneem word met 'n frekwensie van ≥1% die behandelingsgroep met sitagliptien en meer gereeld as die groep met placebo het hipoglykemie gehad (sitagliptien - 10,9%, placebo - 5,2%). In 'n ander studie van 24 weke waarin pasiënte sitagliptien as aanvullende terapie met insulienterapie (met of sonder metformien) ontvang het, was die enigste nadelige reaksie waargeneem met 'n frekwensie van ≥ 1% in die behandelingsgroep met sitagliptien en metformien, en meer gereeld as in die placebo-groep en metformien was braking (sitagliptien en metformien - 1,1%, placebo en metformien - 0,4%).
In 'n algemene analise van 19 dubbelblinde, gerandomiseerde kliniese toetse met die gebruik van sitagliptien (teen 'n dosis van 100 mg / dag) of 'n kontrole-middel (aktief of placebo), was die voorkoms van akute pankreatitis 0,1 gevalle per 100 pasiëntjare behandeling in elke groep (sien "Maatstawwe" voorsorgmaatreëls ").
Geen kliniese beduidende afwykings in vitale tekens of EKG (insluitend die duur van die QTc-interval) is waargeneem met gekombineerde terapie met sitagliptien en metformien nie.
Nadelige reaksies as gevolg van die gebruik van sitagliptien
Pasiënte het geen newe-reaksies ondervind nie as gevolg van sitagliptien, waarvan die frekwensie ≥1% was.
Nadelige reaksies as gevolg van die gebruik van metformien
Die newe-reaksies wat in die metforminegroep by> 5% van die pasiënte en meer gereeld as in die placebo-groep waargeneem word, is diarree, naarheid / braking, winderigheid, astenie, dyspepsie, ongemak in die buik en hoofpyn.
Tydens monitering van die gebruik van die kombinasie van metformien + sitagliptien of sitagliptien, wat deel uitmaak van die registrasie, is monopolie en / of in kombinasie met ander hipoglisemiese middels aan die lig gebring. Aangesien hierdie gegewens vrywillig verkry is uit 'n populasie van 'n onseker grootte, kan die frekwensie en oorsaaklike verband van hierdie nadelige gebeure met terapie nie bepaal word nie. Hierdie nadelige gevolge is onder andere hipersensitiwiteitsreaksies anafilakse, angio-edeem, veluitslag, urtikaria, velkulitis in die vel, eksfoliatiewe velsiektes, insluitend Stevens-Johnson-sindroom, akute pankreatitis, insluitend hemorragiese en nekrotiese vorms met 'n dodelike en nie-dodelike uitkoms, verswakte nierfunksie, insluitend akute nierversaking (dialise word soms benodig ), infeksie in die boonste lugweë, nasofaryngitis, hardlywigheid, braking, hoofpyn, artralgie, myalgie, pyn in die ledemate, rugpyn, jeuk.
Laboratoriumveranderings
Sitagliptin. Die frekwensie van afwykings van laboratoriumparameters in die behandelingsgroepe met sitagliptien en metformien was vergelykbaar met die frekwensie in die behandelingsgroepe met placebo en metformien. Die meeste, maar nie alle kliniese studies nie, het 'n geringe toename in die aantal witbloedselle opgemerk (ongeveer 200 / μl vergeleke met placebo, die gemiddelde inhoud aan die begin van die behandeling 6600 / μl), as gevolg van 'n toename in die aantal neutrofiele. Hierdie verandering word nie as klinies beduidend beskou nie.
Metformin. In gekontroleerde kliniese studies van metformien wat 29 weke duur, is 'n afname in die normale konsentrasie sianokobalamien (vitamien B)12) tot subnormale waardes in bloedserum by ongeveer 7% van die pasiënte, sonder kliniese manifestasies. 'N Soortgelyke afname as gevolg van selektiewe wanabsorpsie van vitamien B12 (naamlik 'n skending van die vorming van 'n kompleks met die interne faktor Castle wat nodig is vir die opname van vitamien B12) lei baie selde tot die ontwikkeling van bloedarmoede en word dit maklik reggestel deur die afskaffing van metformien of 'n ekstra inname van vitamien B12 (sien "Voorsorgmaatreëls").
Interaksie
Sitagliptien en metformien
Die gelyktydige toediening van meerdere dosisse sitagliptien (50 mg 2 keer per dag) en metformien (1000 mg 2 keer per dag) het nie gepaard gegaan met betekenisvolle veranderinge in die farmakokinetiese parameters van sitagliptien of metformien by pasiënte met tipe 2-diabetes mellitus nie.
Ondersoek is gedoen na die effek van die geneesmiddel op die farmakokinetiese parameters van die kombinasie van metformien + saxagliptien, maar 'n voldoende aantal soortgelyke studies is uitgevoer vir elk van die komponente van die kombinasie - sitagliptin en metformien.
In studies oor interaksies met ander geneesmiddels het sitagliptien nie 'n klinies beduidende effek op die farmakokinetika van metformien, rosiglitazoon, glibenklamied, simvastatien, warfarin of orale voorbehoedmiddels gehad nie. Op grond van hierdie data belemmer sitagliptien nie die isoënsieme van CYP3A4, CYP2C 8 of CYP2C 9. Gegevens in vitro dui aan dat sitagliptien ook nie CYP2D6, CYP1A 2, CYP2C 19 en CYP2B 6 isoënsieme onderdruk nie en ook nie CYP3A4 induseer nie.
Volgens 'n populasie farmakokinetiese analise by pasiënte met tipe 2-diabetes, het gepaardgaande terapie nie 'n klinies beduidende effek op die farmakokinetika van sitagliptien gehad nie. Die studie het 'n aantal medisyne wat die meeste gebruik word deur pasiënte met tipe 2-diabetes mellitus geëvalueer, insluitend hipocholesterolemiese middels (statiene, fibrate, ezetimibe), antiplaatplaatjies (clopidogrel), anti-hipertensiewe medisyne (ACE-remmers, ARA II, beta-blokkers, BKK, hidrochloortiazide, pynstillende middels, antro-antoksien, celoksino ), antihistamiene (cetirizine), protonpompinhibeerders (omeprazol, lansoprazole) en vir die behandeling van erektiele disfunksie (sildenafil).
'N Toename in AUC (11%) sowel as die gemiddelde C is opgemerkMax (18%) digoksien in kombinasie met sitagliptien. Hierdie toename word nie as klinies beduidend beskou nie, maar monitering van die pasiënt word aanbeveel tydens die neem van digoksien.
'N Toename in AUC en C is opgemerkMax sitagliptien met onderskeidelik 29 en 68%, met die gesamentlike enkele orale toediening van saxagliptien in 'n dosis van 100 mg en siklosporien ('n sterk P-gp-remmer) in 'n dosis van 600 mg. Hierdie veranderinge in die farmakokinetiese parameters van sitagliptien is nie klinies beduidend nie.
glibenklamied: In 'n studie van die interaksie tussen enkelvoudige dosisse metformien en glibenklamied by pasiënte met tipe 2-diabetes mellitus, is geen veranderinge in die farmakokinetiese en farmakodinamiese parameters van metformien waargeneem nie. Veranderings in AUC en CMax glibenklamied was baie veranderlik. Onvoldoende inligting ('n enkele dosis) en die inkonsekwentheid van die plasmakonsentrasie van glibenklamied met die waargenome farmakodinamiese effekte bevraagteken die kliniese belang van hierdie interaksie.
furosemied: In 'n studie van die intermedikasie-interaksie van enkel dosisse metformien en furosemied by gesonde vrywilligers, is 'n verandering in die farmakokinetiese parameters van beide geneesmiddels waargeneem. Furosemied verhoog die waarde van CMax metformien in plasma en volbloed met 22%, die AUC-waarde van metformien in volbloed met 15%, sonder om die renale klaring van die geneesmiddel te verander. C waardesMax en AUC van furosemied het op hul beurt met onderskeidelik 31 en 12% afgeneem en T1/2 het met 32% gedaal sonder noemenswaardige veranderinge in renale opruiming van furosemied. Daar is geen inligting oor die intermedikasie-interaksie van twee middels met langdurige gewrigsgebruik nie.
nifedipien: tydens die bestudering van die geneesmiddelinteraksie tussen nifedipien en metformien na 'n enkele dosis medisyne deur gesonde vrywilligers, is 'n toename in plasma C gevindMax en AUC van metformien met onderskeidelik 20 en 9%, asook 'n toename in die hoeveelheid metformien wat deur die niere uitgeskei word. TMax en T1/2 metformin het nie verander nie. Dit is gebaseer op 'n toename in die opname van metformien in die teenwoordigheid van nifedipien. Die effek van metformien op die farmakokinetika van nifedipien is minimaal.
Kationiese preparate: kationiese middels (d.w.s. amiloride, digoksien, morfien, prokaainamied, kinidien, kinien, ranitidien, triamteren, trimethoprim of vankomisien) wat deur buisafskeiding gesekreteer word, kan teoreties in wisselwerking met metformien wees, en meeding om 'n gedeelde nierbuisvormige transportstelsel. 'N Soortgelyke kompetisie is waargeneem met die gelyktydige toediening van metformien en cimetidien deur gesonde vrywilligers in enkel- en meervoudige dosisstudies, met 'n toename van 60% in konsentrasie CMax metformien in plasma en volbloed, en 'n toename van 40% in AUC van metformien in plasma en volbloed. In 'n enkele dosisstudie1/2 metformien het nie verander nie. Metformien het nie die farmakokinetika van cimetidine beïnvloed nie. Alhoewel hierdie inter-geneesmiddelinteraksies hoofsaaklik van teoretiese belang is (met die uitsondering van cimetidien), word sorgvuldig monitering van die pasiënt en dosisaanpassing van die kombinasie van metformin + sitagliptien en / of bogenoemde kationiese medisyne wat deur die proksimale nierbuisies uitgeskei word aanbeveel.
ander: sommige medisyne het hiperglikemiese potensiaal en dit kan die gevestigde beheer van glukemie beïnvloed. Dit sluit in tiasied en ander diuretika, kortikosteroïede, fenotiasiene, skildklierhormone, oestrogenen, orale voorbehoedmiddels, fenoïtien, nikotiensuur, simpatomimetika, BKK en isonisied. Wanneer die voorgeskrewe medisyne voorgeskryf word aan 'n pasiënt wat 'n kombinasie van metformien + sitagliptien ontvang, word aanbeveel dat glukemiese beheerparameters noukeurig gemoniteer word.
Terwyl gesonde vrywilligers metformien en propranolol of metformien en ibuprofen neem, is geen farmakokinetiese parameters van hierdie middels waargeneem nie.
Slegs 'n onbeduidende deel van metformien bind aan plasmaproteïene, daarom is inter-geneesmiddelinteraksies van metformien met geneesmiddels wat aktief bind aan plasmaproteïene (salisilate, sulfanilamiede, chlooramfenikol en probenesied) onwaarskynlik, anders as sulfonylurea, wat ook aan plasmaproteïene bind.
Dosis en toediening
Januvia mag geneem word sonder inagneming van etes.
Die aanvanklike aanbevole dosis is 100 mg een keer per dag.
Geen dosisaanpassing is nodig wanneer Januvia in kombinasie met metformien en / of 'n PPARy-agonis (thiazolidinediones) gebruik word nie. Geneesmiddels moet gelyktydig ingeneem word.
As u Januvia in kombinasie met sulfonylureum of insulien gebruik, kan laer dosisse sulfonylurea of insulien oorweeg word om die risiko van hipoglukemie te verminder.
Wanneer 'n dosis Januvia oorgeslaan word, moet die pasiënt dit neem sodra hy dit onthou. Moenie 'n dubbele dosis van die middel op die dag van opname neem nie.
Pasiënte met nierversaking. Pasiënte met ligte nierversaking (CC ≥50 ml / min, wat ongeveer ooreenstem met 'n plasmakreatinienvlak van ≤1,7 mg / dL by mans, ≤ 1,5 mg / dL by vroue) hoef nie die Januvia-dosis aan te pas nie.
Vir pasiënte met matige nierversaking (CC ≥30 ml / min, maar 1,7 mg / dl, maar ≤3 mg / dl by mans,> 1,5 mg / dl, maar ≤2,5 mg / dl by vroue), is die Januvia-dosis 50 mg een een keer per dag.
Vir pasiënte met ernstige nierversaking (CC 3 mg / dl by mans,> 2,5 mg / dl by vroue), sowel as met 'n terminale stadium van nierpatologie, wat hemodialise of peritoneale dialise benodig, is die dosis Januarie een keer per dag 25 mg. Januvia kan gebruik word ongeag die dialise tyd.
Pasiënte met lewerversaking. Dosisaanpassing is nie nodig vir Januvia by pasiënte met ligte tot matige lewerversaking nie. Die middel is nie bestudeer by pasiënte met ernstige lewerversaking nie.
Bejaarde pasiënte. Geen dosisaanpassing is nodig vir bejaarde pasiënte nie. Die gebruik van Januvia by pasiënte ouer as 75 jaar is nie bestudeer nie.
Kinders se ouderdom. Dit word nie aanbeveel om Januvia te gebruik vir kinders en adolessente onder die ouderdom van 18 nie, as gevolg van die gebrek aan kliniese studies oor veiligheid en effektiwiteit in hierdie ouderdomsgroep.
Moontlikheid van ingewikkelde toepassing
Sitagliptien belemmer nie die aktiwiteit van Rosiglitazone, Simvastatin, Metformin en Warfarin nie. Dit kan gebruik word deur vroue wat gereeld orale voorbehoedmiddels gebruik. As dit parallel met Dioxin voorgeskryf word, word die moontlikhede van laasgenoemde effens verbeter, maar sulke veranderinge hoef nie die dosis aan te pas nie.
'Sitagliptin' word gelyktydig met remmers gebruik (byvoorbeeld met 'Ketoconazole') en met siklosporien. Die effek van die middel in sulke situasies is nie krities nie en verander nie die voorwaardes vir die gebruik daarvan nie.
Aangesien daar by die behandeling van tipe 2-diabetes 'n dubbele las op die niere gedoen word, met die keuse van 'n kompleks van medisyne, is dit nodig om hul vermoëns en toestand in ag te neem.
"Sitagliptin" is die internasionale naam van die dwelm, en die handelsinonieme daarvan is "Januvia."

Tydens kliniese toetse het medikasie gebaseer op sitagliptien geen beduidende en beduidende effek op die farmakologiese kinetika van Rosiglitazon, Simvastatin, Metformin, orale voorbehoedmiddels, Warfarin en Glibenclamide gehad nie.
By die gebruik van preparate wat op sitagliptien gebaseer is, vind inhibisie van isoënsieme CYP2C9, CYP3A4 en CYP2C8 nie plaas nie. Boonop inhibeer hierdie middels nie die volgende ensieme nie: CYP2C19, CYP1A2, CYP2B6 en CYP2D6. ”
Die gelyktydige gebruik van "Metformin" en "Sitagliptin" bring nie beduidende veranderinge in die farmakokinetika van die aktiewe stof van laasgenoemde in diabetes mellitus mee nie.
Die gekombineerde Yanumet kan beskou word as 'n analoog van Sitagliptinum Sitagliptin, dit bevat metformien en sitagliptien.
Daar is 'n middel met dieselfde aktiewe stowwe - metformien en sitagliptien - dit "Velmetiya". Ander analoë van "Yanumet" het 'n soortgelyke aksie en ATC-kode:
- "Avandamet"
- "Glibomet"
- "Duglimaks"
- "Triprayd".
In ooreenstemming met die oorsigte van pasiënte wat hierdie medisyne vir behandeling gebruik, beïnvloed dit die suikervlak in die menslike liggaam, maar hulle benodig streng beheer van die toestand as gevolg van die moontlike voorkoms van baie newe-effekte.

Die koste van die medisyne hang af van die verpakking en die landstreek. Wissel tussen 1596-1724 roebels. Die prys van die analoog van Sitagliptin Yanumet is vanaf 1.680 roebels.
Volgens berigte op verskillende forums word die medisyne in 'n vroeë stadium van die patologie aan diabete voorgeskryf. Die beoordelings van spesialiste en pasiënte toon dat daar 'n groot aantal subtiliteite bestaan in die gebruik van incretinomimetic.
"Sitagliptin" is 'n nuwe generasie middel, nie alle dokters het baie ervaring in die gebruik daarvan nie. Tot onlangs was Metformin wyd gebruik, maar nou word Januvia as monoterapie voorgeskryf. Met 'n voldoende aantal moontlikhede is dit onvanpas om dit met medisyne soos Metformin aan te vul.

Die analoog van “Sitagliptin” “Yanumet” word getoon as 'n toevoeging tot die regime van fisieke aktiwiteit en dieet, wat bydra tot die beter beheer van glukemie in tipe 2-diabetes. Resensies oor hom is meestal positief.Diabete sê egter dat die middel en die analoë daarvan nie altyd aan al die vereistes voldoen nie, maar die doeltreffendheid daarvan neem mettertyd af. Die punt hier is nie verslawing nie, maar die kenmerke van die siekte: die tweede tipe diabetes is 'n chroniese patologie wat aan die gang is.
Ons het die prys, resensies en analoë van die geneesmiddel “Sitagliptin” nagegaan.
Oordosis
Gedurende kliniese proewe is 'n enkele dosis sitagliptien in 'n dosis van tot 800 mg gewoonlik goed verdra deur gesonde vrywilligers. Minimale veranderinge in die QT-interval, wat nie as klinies beduidend beskou word nie, is waargeneem in een van die studies van sitagliptien in 'n daaglikse dosis van 800 mg (sien "Farmakodinamika", Effek op elektrofisiologie van die hart). 'N Dosis van meer as 800 mg per dag by mense is nie bestudeer nie.
In kliniese proewe met herhaalde toediening van sitagliptien (fase I), is geen newe-reaksies wat verband hou met die behandeling met sitagliptien waargeneem met 'n daaglikse dosis van tot 400 mg vir 28 dae nie.
In geval van 'n oordosis, is dit nodig om standaard ondersteunende maatreëls te begin: verwydering van die nog nie-geabsorbeerde sitagliptien uit die spysverteringskanaal, monitering van vitale tekens, insluitend EKG, en die aanstelling van simptomatiese terapie indien nodig.
Sitagliptien is swak gedialiseer: volgens kliniese studies is slegs 13,5% van die dosis tydens 'n 3-4-uur dialisesessie uitgeskei. In die geval van kliniese nood, word langdurige hemodialise voorgeskryf. Daar is geen inligting oor die effektiwiteit van peritoneale dialise nie.
Daar was gevalle van oordosis metformien, insluitend toediening in meer as 50 g (50.000 mg). In ongeveer 10% van alle gevalle van oordosis is hipoglisemie waargeneem, maar 'n duidelike verband met 'n oordosis metformien is nie vasgestel nie. Die ontwikkeling van melksuurdosis het gepaard gegaan met ongeveer 32% van alle gevalle van oordosis metformien (sien "Voorsorgmaatreëls", metformien). 'N Nood-hemodialise is moontlik (metformien word gedialiseer teen 'n snelheid van tot 170 ml / min onder goeie hemodinamika) om die eliminasie van oortollige metformien te versnel in geval van vermoedelike oordosis.
Voorsorgmaatreëls Metformin + Sitagliptin
Metformin + Sitagliptin-kombinasie
In die waarnemingstydperk na registrasie is daar verslae ontvang oor die ontwikkeling van akute pankreatitis, insluitend hemorragies of nekroties met dodelike en nie-dodelike uitslag, by pasiënte wat sitagliptien neem (sien "newe-effekte", Waarnemings na registrasie).
Aangesien hierdie boodskappe vrywilliglik ontvang is van 'n populasie van onsekerheid, is dit onmoontlik om die frekwensie van hierdie boodskappe betroubaar te skat of om 'n oorsaaklike verband met die duur van die middel te bepaal. Pasiënte moet ingelig word oor die kenmerkende simptome van akute pankreatitis: aanhoudende erge buikpyn. Kliniese manifestasies van pankreatitis het verdwyn na staking van sitagliptien. In die geval van vermoedelike pankreatitis, is dit nodig om op te hou met die kombinasie van metformien + sitagliptien en ander potensieel gevaarlike middels.
Nierfunksie monitering
Die verkieslike roete om metformien en sitagliptien te elimineer, is uitskeiding van niere. Die risiko van ophoping van metformien en die ontwikkeling van melksuuridose neem toe in verhouding tot die mate van verswakte nierfunksie, daarom moet die kombinasie van metformin + sitagliptin nie voorgeskryf word aan pasiënte met 'n serumkreatinienkonsentrasie hoër as die ouderdomsverwante VGN nie. As gevolg van 'n ouderdomsverwante afname in nierfunksie, moet bejaarde pasiënte daarna streef om voldoende glukemiese beheer te verkry teen die minimum dosis metformien + sitagliptien kombinasie. By ouer pasiënte, veral diegene ouer as 80, monitor hulle die nierfunksie gereeld. Voordat die behandeling met 'n kombinasie van metformien + sitagliptien begin word, en ook ten minste een keer per jaar na die aanvang van die behandeling, met behulp van toepaslike toetse, bevestig dit die normale nierfunksie.Met 'n verhoogde waarskynlikheid om nierfunksie te ontwikkel, word die nierfunksie meer gereeld uitgevoer, en as dit opgespoor word, word die kombinasie van metformin + sitagliptien gekanselleer.
Die ontwikkeling van hipoglukemie met gelyktydige gebruik met sulfonylurea of insulien
Soos met ander hipoglukemiese middels, is hipoglisemie waargeneem met die gelyktydige gebruik van sitagliptien en metformien in kombinasie met insulien- of sulfonielureumderivate (sien “newe-effekte”). Om die risiko van sulfoniel-geïnduseerde of insulien-geïnduseerde hipoglisemie te verminder, moet die dosis sulfonielureumderivaat of insulien verminder word.
Die ontwikkeling van hipoglukemie met gelyktydige gebruik met sulfonylurea of insulien
In kliniese studies van sitagliptien, beide in monoterapie en in kombinasie met medisyne wat nie lei tot die ontwikkeling van hipoglukemie nie (d.w.z. metformien of PPARy-agoniste - thiazolidinediones), was die voorkoms van hipoglykemie in die groep pasiënte wat sitagliptien neem, naby die frekwensie in die groep pasiënte. neem 'n placebo. Soos met ander hipoglykemiese middels, is hipoglisemie waargeneem met die gelyktydige gebruik van sitagliptien in kombinasie met insulien- of sulfonielureumderivate (sien “newe-effekte”). Om die risiko van sulfoniel-geïnduseerde of insulien-geïnduseerde hipoglisemie te verminder, moet die dosis sulfonielureumderivaat of insulien verminder word.
By monoterapie en / of in kombinasie met ander hipoglikemiese middels, is hipersensitiwiteitsreaksies tydens monitering en / of in kombinasie met ander hipoglikemiese middels opgemerk. Hierdie reaksies het anafilakse, angio-oedeem, eksfoliatiewe velsiektes, insluitend Stevens-Johnson-sindroom, ingesluit. Aangesien hierdie gegewens vrywillig verkry is uit 'n populasie van onseker grootte, kan die frekwensie en oorsaaklike verband met die behandeling van hierdie newe-reaksies nie bepaal word nie. Hierdie reaksies het gedurende die eerste 3 maande na die aanvang van die behandeling met sitagliptien plaasgevind, sommige is waargeneem na die eerste dosis. As vermoed word dat die ontwikkeling van 'n hipersensitiwiteitsreaksie is, is dit nodig om op te hou om die kombinasie van metformin + sitagliptien te neem, ander moontlike oorsake van die nadelige voorkoms te evalueer en ander lipiedverlagende terapie voor te skryf (sien "Kontraïndikasies" en "newe-effekte", Waarnemings na registrasie).
Melksuuradidose is 'n seldsame maar ernstige metaboliese komplikasie wat ontstaan as gevolg van die ophoping van metformien tydens behandeling met die kombinasie van metformien + sitagliptien. Sterftes by melksuurdosis bereik ongeveer 50%. Die ontwikkeling van melksuurdosis kan ook op die agtergrond van sommige somatiese siektes voorkom, veral diabetes mellitus of enige ander patologiese toestand, gepaard met ernstige hipoperfusie en hipoksemie van weefsels en organe. Melksuuratose word gekenmerk deur 'n verhoogde konsentrasie van laktaat in die bloedplasma (> 5 mmol / l), 'n verlaagde pH in die bloed, elektrolietversteurings met 'n toename in die aniooninterval, 'n toename in die verhouding van laktaat / pirovaat. As metformien die oorsaak van asidose is, is die plasmakonsentrasie gewoonlik> 5 μg / ml. Volgens berigte het melksuuradidose by die behandeling van metformien baie selde ontwikkel (in ongeveer 0,03 gevalle per 1000 pasiëntjare, met 'n sterftesyfer van ongeveer 0,015 gevalle per 1000 pasiëntjare). Gedurende 20.000 pasiënte-jaar metformienbehandeling is geen gevalle van melksuurdosis in kliniese studies aangemeld nie.Bekende gevalle het hoofsaaklik voorgekom by pasiënte met diabetes mellitus met ernstige nierversaking, insluitend ernstige patologie en nierhypoperfusie, dikwels in kombinasie met gepaardgaande veelvuldige somatiese / chirurgiese siektes en polyfarmasie. 'N Beduidende verhoogde risiko vir melksuuradidose by pasiënte met hartversaking wat beduidende regstelling van medisyne benodig, veral met onstabiele angina pectoris / hartversaking in die akute stadium, gepaard met erge hipoperfusie en hipoksemie. Die risiko om melksuurdosis te ontwikkel neem toe in verhouding tot die mate van verswakte nierfunksie en die ouderdom van die pasiënt. Daarom kan voldoende monitering van nierfunksie, sowel as die gebruik van die minimum effektiewe dosis metformien, die risiko van melksuurdosis aansienlik verminder. Noukeurige monitering van nierfunksie is veral nodig by die behandeling van bejaarde pasiënte, en vir pasiënte ouer as 80 jaar begin die behandeling met metformien eers na bevestiging van voldoende nierfunksie volgens die resultate van die kreatinienopruiming, aangesien hierdie pasiënte meer gevaar het om melksuurdosis te ontwikkel. Boonop moet metformin onmiddellik gekanselleer word in enige toestand wat gepaard gaan met die ontwikkeling van hipoksemie, dehidrasie of sepsis. Aangesien die uitskeiding van laktaat met 'n verminderde lewerfunksie aansienlik verminder word, moet metformien nie aan pasiënte met kliniese of laboratoriumtekens van lewersiekte voorgeskryf word nie. Tydens die behandeling met metformien, moet alkoholinname beperk word, aangesien alkohol die effek van metformien op die laktaatmetabolisme versterk. Boonop word die behandeling met metformien tydelik gestaak vir die duur van intravaskulêre radiopaque studies en chirurgiese ingrepe.
Die aanvang van melksuurdosis is dikwels moeilik om op te spoor, en dit gaan gepaard met slegs nie-spesifieke simptome, soos malaise, myalgie, respiratoriese noodsindroom, verhoogde slaperigheid en nie-spesifieke dispeptiese simptome. Met die verergering van die laktiese asidose kan hipotermie, arteriële hipotensie en weerstandige bradyaritmie by bogenoemde simptome aansluit. Die dokter en die pasiënt moet bewus wees van die moontlike belang van sulke simptome, en die pasiënt moet die dokter onmiddellik inlig oor hul voorkoms. Behandeling met metformien word gekanselleer totdat die situasie opklaar.
Plasmakonsentrasies van elektroliete, ketone, bloedglukose word bepaal, sowel as (volgens aanduidings) die pH-waarde van die bloed, die konsentrasie van laktaat. Soms kan inligting oor plasma-metformienkonsentrasie ook nuttig wees. Nadat die pasiënt gewoond is aan die optimale dosis metformien, moet die spysverteringstelsel simptome kenmerkend van die aanvanklike stadiums van die behandeling verdwyn. As sulke simptome voorkom, is dit waarskynlik 'n teken van die ontwikkeling van melksuurdosis of 'n ander ernstige siekte.
As die konsentrasie van laktaat in die veneuse bloedplasma tydens behandeling met metformien meer is as VGN, wat nie hoër as 5 mmol / l is nie, is dit nie patognomonies vir melksuurdosis nie, en kan dit te wyte wees aan toestande soos swak beheerde diabetes mellitus of vetsug, of oormatige fisieke inspanning, of 'n tegniese metingsfout . In enige pasiënt met diabetes mellitus en metaboliese asidose, in die afwesigheid van 'n bevestiging van ketoasidose (ketonuria en ketonemie), bestaan die risiko vir melksuurdosis.
Melksuuratose is 'n toestand wat noodsorg in 'n mediese fasiliteit benodig. Metformienbehandeling word gekanselleer en die nodige maatreëls vir onderhoudsterapie word onmiddellik uitgevoer. Aangesien metformien met 'n snelheid van tot 170 ml / min gedialiseer word onder toestande van goeie hemodinamika, word onmiddellike hemodialise aanbeveel om asidose vinnig te korrigeer en opgehoopte metformien te verwyder.Hierdie maatreëls lei dikwels tot die vinnige verdwyning van alle simptome van melksuurdosis en die herstel van die toestand van die pasiënt (sien "Kontraïndikasies").
Onder normale omstandighede, met metformien monoterapie, ontwikkel hipoglukemie nie, maar die ontwikkeling daarvan is moontlik teen die agtergrond van die honger, na aansienlike fisieke inspanning sonder die daaropvolgende vergoeding van kalorieë wat verbruik word, terwyl die gebruik van ander hipoglykemiese middels (sulfonylureumderivate en insulien) of alkohol. Die ontwikkeling van hipoglykemie beïnvloed in 'n groter mate ouer, verswakte of uitgeputte pasiënte, pasiënte wat alkohol misbruik, pasiënte met bynier- of pituïtêre insuffisiënt. Hipoglykemie is moeilik te herken by bejaarde pasiënte en pasiënte wat beta-blokkeerders neem.
Gelyktydige farmakoterapie kan die nierfunksie of metformien verspreiding benadeel. Die gelyktydige gebruik van medisyne wat die nierfunksie, hemodinamika of die verspreiding van metformien nadelig beïnvloed (soos kationiese middels wat deur die buisafskeiding uit die liggaam geskei word), moet met omsigtigheid voorgeskryf word (sien "Interaksie", metformien).
Radiologiese studies met intravaskulêre toediening van jodiumbevattende kontrasmiddels (bv. Iv-urografie, iv-cholangiografie, angiografie, rekenaartomografie en iv-toediening van kontrasmiddels)
Intravaskulêre toediening van jodiumbevattende kontrasmiddels hou verband met die ontwikkeling van melksuurdosis by pasiënte wat metformien neem, en dit kan akute nierfunksie veroorsaak (sien "Kontraïndikasie"). Daarom moet pasiënte wat vir so 'n studie geskeduleer is, 48 uur voor en binne 48 uur na die studie tydelik ophou om die kombinasie van metformien + sitagliptien te neem. Die hervatting van die behandeling is slegs toelaatbaar nadat laboratoriumbevestiging van normale nierfunksie bevestig is.
Vaskulêre ineenstorting (skok) van enige etiologie, akute hartversaking, akute miokardiale infarksie en ander toestande wat gepaard gaan met die ontwikkeling van hipoksemie, kan die ontwikkeling van melksuurdosis en nierasotemie veroorsaak. As die genoemde toestande by die pasiënt ontwikkel tydens behandeling met die kombinasie van metformien + sitagliptien, moet die kombinasie onmiddellik gestaak word.
Die gebruik van die kombinasie van metformin + sitagliptien moet gestaak word vir die duur van enige chirurgiese ingreep (met die uitsondering van klein manipulasies wat nie die drinkregime en honger beperk nie) en totdat die normale maaltyd hervat word, mits laboratoriumbevestiging van normale nierfunksie verkry word.
Alkohol versterk die effek van metformien op melksuurmetabolisme. Die pasiënt moet gewaarsku word oor die gevare van alkoholmisbruik ('n enkele dosis groot hoeveelhede of die konstante inname van klein dosisse) gedurende die behandelingstydperk met die kombinasie van metformien + sitagliptien.
Verswakte lewerfunksie
Aangesien daar gevalle bekend is van die ontwikkeling van melksuurdosis by pasiënte met 'n verminderde lewerfunksie, word dit nie aanbeveel om 'n kombinasie van metformien + sitagliptien voor te skryf vir pasiënte met kliniese of laboratoriumtekens van lewersiekte nie.
Die konsentrasie van sianokobalamien (vitamien B12) in bloedplasma
In gekontroleerde studies van metformien wat 29 weke duur, toon 7% van die pasiënte 'n afname in die aanvanklike normale konsentrasie sianokobalamien (vitamien B12) in bloedplasma sonder die ontwikkeling van kliniese simptome van tekort. 'N Soortgelyke afname kan wees as gevolg van selektiewe wanabsorpsie van vitamien B12 (naamlik 'n oortreding van die vorming van die kompleks met die interne faktor Castle wat nodig is vir die opname van vitamien B12) lei baie selde tot die ontwikkeling van bloedarmoede en word dit maklik reggestel deur die afskaffing van metformien of 'n ekstra inname van vitamien B12. By behandeling met die kombinasie van metformin + sitagliptien, word dit aanbeveel om die hematologiese parameters van die bloed jaarliks te kontroleer, en enige afwykings wat ontstaan het, moet bestudeer en reggestel word. Pasiënte met vitamien B-tekorte12 (as gevolg van verminderde inname of opname van vitamien B12 of kalsium) word dit aanbeveel om die plasmakonsentrasie van vitamien B te bepaal12 met tussenposes van 2-3 jaar.
Verandering in die kliniese status van pasiënte met 'n voldoende beheerde tipe 2-diabetes mellitus
Indien laboratoriumafwykings of kliniese simptome van die siekte (veral 'n toestand wat nie duidelik geïdentifiseer kan word nie) by 'n pasiënt met voorheen voldoende beheerde tipe 2-diabetes mellitus voorkom, moet onmiddellik onmiddellik uitgesluit word. Die beoordeling van die toestand van die pasiënt behoort bloedtoetse vir elektroliete en ketone, die konsentrasie van glukose in die bloed, sowel as (volgens aanduidings), die pH van die bloed, die plasmakonsentrasies van laktaat, pirovaat en metformien, in te sluit. Met die ontwikkeling van asidose van enige etiologie, moet u dadelik ophou om die kombinasie van metformien + sitagliptien te neem en toepaslike maatreëls tref om asidose reg te stel.
Verlies aan glukemiese beheer
In situasies van fisiologiese spanning (hipertermie, trauma, infeksie of chirurgie) by 'n pasiënt met voorheen stabiele glukemiese beheer, is 'n tydelike verlies aan glukemiese beheer moontlik. In sulke periodes is 'n tydelike vervanging van die kombinasie van metformien + sitagliptien met insulienterapie aanvaarbaar, en na die oplossing van die akute situasie kan die pasiënt die vorige behandeling hervat.
Beïnvloed die vermoë om voertuie te bestuur en met meganismes te werk. Geen studies is gedoen om die effek van die kombinasie van metformin + sitagliptien op die vermoë om voertuie te bestuur en met meganismes te bestudeer, te ondersoek nie. Nietemin, gevalle van duiseligheid en slaperigheid wat tydens sitagliptien geneem word, moet in ag geneem word.
Daarbenewens moet pasiënte bewus wees van die risiko van hipoglykemie, terwyl hulle 'n kombinasie van metformien + sitagliptien en sulfonielureumderivate of insulien gebruik.
Materiële monsternemingsreëls en normale glukose-lesings
Normale vaswaardes vir volbloed - 3,3-5,5 mmol / L, vir plasma - 4,0-6,1 mmol / L.
Bloedmonsterneming vir hierdie eenvoudige analise het sy eie subtiliteite. Bloed, hetsy veneus of kapillêr, moet soggens op 'n leë maag vir ontleding geneem word. Jy kan nie tien uur eet nie, jy kan skoon water drink, maar voor dit moet die kos bekend wees.

Onmiddellik voor manipulasie is dit nodig om spanning, onrus, liggaamlike aktiwiteit te vermy; u kan nie rook nie. Die resultaat kan beïnvloed word deur sekere groepe medisyne (salisilate, individuele verteenwoordigers van antibiotika), vitamien C, sowel as sommige ander medisyne, siektes en toestande wat aan die behandelende dokter gerapporteer moet word.
'N Studie wat aanbeveel word vir sifting, is vaste suiker. Met 'n redelik vinnige en eenvoudige metode kan u groot bevolkingsgroepe ondersoek na die verminderde koolhidraatmetabolisme. Hierdie analise verwys na diegene wat sonder die voorskrif van 'n dokter uitgevoer kan word. Dit is veral belangrik om bloed van 'n vinger vir suiker te skenk aan mense wat die risiko het vir tipe 2-diabetes.
Sitagliptien om eetlus en liggaamsgewig diabetes te beheer
In die patogenese van tipe 2-diabetes word drie hoofmeganismes onderskei:
- Weefselinsulienweerstand,
- Versteurings in die produksie van endogene insulien,
- Oormatige sintese van glukose deur die lewer.
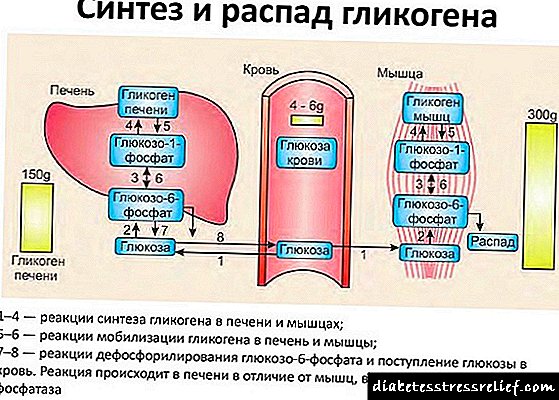
Verantwoordelikheid vir die ontwikkeling van so 'n verraderlike siekte lê by b- en c-selle van die pankreas. Laasgenoemde produseer ook 'n hormoon wat die omskakeling van glukose in energie vir spiere en die brein stimuleer. As die tempo van die produksie daal, veroorsaak dit hiperglikemie.
B-selle is verantwoordelik vir die produksie van glukagon, die oormaat daarvan skep die voorvereistes vir die oormatige afskeiding van glukose deur die lewer. Oormatige glukagon en 'n gebrek aan insulien bied die voorwaardes vir die ophoping van onverwerkte glukose in die bloedstroom.
Doeltreffende bestuur van tipe 2-diabetes is nie moontlik sonder 'n stabiele en langdurige (vir die hele periode van die siekte) beheer van koolhidraatmetabolisme nie. Talle internasionale proewe bevestig dat slegs suikervergoeding die voorwaardes bied vir die voorkoming van komplikasies en die lewensverwagting van 'n diabeet verhoog.
Ondanks al die verskillende antidiabetiese middels, slaag nie alle pasiënte met hul hulp om 'n stabiele kompensasie van koolhidrate te verkry nie. Volgens 'n gesaghebbende UKPDS-studie het 45% van diabete na 3 jaar 100% vergoeding ontvang vir die voorkoming van mikroangiopatie, en slegs 30% na 6 jaar.
Hierdie probleme bepaal die noodsaaklikheid om 'n fundamenteel nuwe klas medisyne te ontwikkel wat nie net metaboliese probleme kan uitskakel nie, maar ook die pankreas kan onderhou, wat die fisiologiese meganisme stimuleer wat u in staat stel om die produksie van insulien en glukemie te reguleer.
Die medisyne met die inkretien wat tipe 2-diabetes kan beheer sonder om die pankreas te stimuleer, skielike veranderinge in glukemie, die risiko van hipoglukemie is die nuutste ontwikkeling deur aptekers.
Die GLP-4-ensieminhibeerder Sitagliptin help 'n diabeet om die eetlus en liggaamsgewig te beheer, en bied die liggaam die vermoë om die probleem van glukose-toksisiteit onafhanklik te oorkom.
Stel vorm en komposisie vry
 Die middel gebaseer op sitagliptien met die handelsnaam Januvia is beskikbaar in die vorm van ronde tablette met 'n pienk of beige kleur en gemerk “227” vir 100 mg, “112” vir 50 mg, “221” vir 25 mg. Die tablette word verpak in plastiekkaste of in potloodsakkies. Daar kan verskillende borde in 'n boksie wees.
Die middel gebaseer op sitagliptien met die handelsnaam Januvia is beskikbaar in die vorm van ronde tablette met 'n pienk of beige kleur en gemerk “227” vir 100 mg, “112” vir 50 mg, “221” vir 25 mg. Die tablette word verpak in plastiekkaste of in potloodsakkies. Daar kan verskillende borde in 'n boksie wees.
Die basiese aktiewe stof sitagliptienfosfaathidraat word aangevul met croscarmellose-natrium, magnesiumstearaat, sellulose, natriumstearielfumarat, ongeraffineerde kalsiumwaterstoffosfaat.
Vir sildagliptin hang die prys van die pakket af, veral vir 28 tablette wat u moet betaal 1,596-1724 roebels. 'N Voorskrifmedikasie word gegee, die rakleeftyd is 1 jaar. Die medisyne benodig geen spesiale voorwaardes vir opberging nie. Oop verpakking word vir 'n maand op die yskasdeur gestoor.
Farmakokinetika van sitagliptien
Die opname van die geneesmiddel vind vinnig plaas, met 'n biobeskikbaarheid van 87%. Die absorpsietempo is nie afhanklik van die tyd van inname en samestelling van die voedsel nie, veral die vetterige voedsel verander nie die farmakokinetiese parameters van die incretin mimetic nie.
In ewewig verhoog die ekstra gebruik van 'n 100 mg tablet die oppervlakte onder die AUC-kromme, wat die afhanklikheid van die verspreidingsvolumes betyds met 14% kenmerk. 'N Enkele dosis van 100 mg tablette waarborg 'n verspreidingsvolume van 198 l.
'N Relatiewe klein deel van die inkretienmimetika word gemetaboliseer. Ses metaboliete is geïdentifiseer wat nie die vermoë het om DPP-4 te inhibeer nie. Nieropruiming (QC) - 350 ml / min. Die grootste deel van die middel word deur die niere geëlimineer (79% in onveranderde vorm en 13% in die vorm van metaboliete), die res word deur die ingewande geskei.
In die lig van die swaar las op die niere by diabete met 'n chroniese vorm (CC - 50-80 ml / min.), Is die aanwysers identies met CC 30-50 ml / min. 'n verdubbeling van die AUC-waardes is waargeneem, met CC onder 30 ml / min. - vier keer. Sulke toestande dui op dosis titrasie.
Met lewepatologieë van matige erns verhoog Cmax en AUC met 13% en 21%. In ernstige vorme verander die farmakokinetika van sitagliptien nie noemenswaardig nie, aangesien die geneesmiddel hoofsaaklik deur die niere uitgeskei word.
Wie word incretinomimetic getoon
Die medikasie word voorgeskryf vir tipe 2-diabetes, benewens 'n lae-koolhidraatdieet en voldoende spieraktiwiteit.
Dit word gebruik as 'n enkele middel en gesamentlike terapie met metformien, sulfonylurea preparate of tiazolidinedione. Dit is ook moontlik om insulieninspuitingsmetodes te gebruik as hierdie opsie help om die probleem van insulienweerstandigheid op te los.
Vir die behandeling van gewrigte het ons lesers DiabeNot suksesvol gebruik. Aangesien die produk gewild is, het ons besluit om dit onder u aandag te bring.
Nadelige gebeure
Te oordeel na die resensies is die meeste van alle diabete besorg oor dyspepsie, ontstelde ontlasting. In laboratoriumtoetse word hiperurisemie, 'n afname in die doeltreffendheid van die tiroïedklier en leukositose opgemerk.
Onder ander onvoorsiene effekte (daar is nie 'n verband met incretinimimetika nie) - respiratoriese infeksies, artralgie, migraine, nasofaryngitis). Die voorkoms van hipoglisemie is soortgelyk aan die resultate by die kontrolegroep wat placebo ontvang het.
Geneesmiddelinteraksie-resultate
Met die gelyktydige gebruik van sitagliptien met metformien, rosiglitazoon, orale voorbehoedmiddels, glibenklamied, warfarien, simvastatien, verander die farmakokinetika van hierdie groep geneesmiddels nie.
Gelyktydige toediening van sitagliptien en digoksien impliseer nie 'n verandering in die dosis van medikasie nie. Soortgelyke aanbevelings word aangebied deur die instruksie en interaksie van sitagliptien en siklosporien, ketoconazole.
Sildagliptin - analoë
Sitagliptin is die internasionale naam vir die middel; die handelsnaam is Januvius. 'N Analoog kan beskou word as die gekombineerde medikasie Yanumet, wat sitagliptien en metformien insluit. Galvus behoort tot die groep DPP-4-remmers (Novartis Pharma AG, Switserland) met die aktiewe komponent vildagliptin, prys 800 roebels.
Hipoglykemiese middels is ook geskik vir die ATX-kode van vlak 4:
- Nesina (Takeda Pharmaceuticals, VSA, gebaseer op alogliptien),
- Onglisa (Bristol-Myers Squibb Company, gebaseer op saxagliptien, prys - 1800 roebels),
- Trazhenta (Bristol-Myers Squibb Company, Italië, Brittanje, met die aktiewe stof linagliptin), prys - 1700 roebels.
Hierdie ernstige medisyne is nie in die lys van voorkeursmedisyne opgeneem nie, is dit die moeite werd om op u eie risiko te eksperimenteer en u begroting en u gesondheid te waag?
Sitagliptin resensies
Te oordeel na berigte oor tematiese forums word Januarie in die beginfase van die siekte dikwels aan diabete voorgeskryf. Oor sitagliptien toon resensies van dokters en pasiënte dat die gebruik van incretinomimetic baie nuanses het.
Januvia is 'n nuwe generasie medisyne en nie alle dokters het genoeg ervaring opgedoen met die gebruik daarvan nie. Tot onlangs was metformien die eerste-lyn-middel; nou word Januvia ook as monoterapie voorgeskryf. As dit voldoende is, is dit nie raadsaam om dit met metformien en ander medisyne aan te vul nie.
Diabetici kla dat die medisyne nie altyd aan die vereiste vereistes voldoen nie, maar mettertyd neem die effektiwiteit daarvan af. Die probleem hier is om nie aan die pille gewoond te raak nie, maar aan die eienskappe van die siekte: tipe 2-diabetes - 'n chroniese, progressiewe patologie.
Alle opmerkings lei tot die gevolgtrekking dat die bekendstelling in die kliniese praktyk van sitagliptien, wat 'n fundamentele nuwe klas medisyne is, ruim geleentheid bied vir die bestuur van tipe 2-diabetes op enige stadium, van prediabetes tot bykomende terapie, met onbevredigende resultate van die toepassing van tradisionele glukemiese kompensasiestelsels.
Verslag deur professor A.S. Ametov, endokrinoloog-diabetoloog oor die teorie en praktyk van die gebruik van sitagliptien - op video.
Lekkers vir diabetes
Die vraag rakende die gebruik van suikergoedprodukte deur pasiënte met suikersiekte bly, indien nie die meeste nie, dan die belangrikste vir baie dekades. Ongetwyfeld het almal wat nie eens een keer in hul lewe met hierdie endokriene siekte siek was nie, gehoor dat lekkers skadelik is vir diabete en dat dit die liggaam onherstelbare skade kan berokken.Moet egter nie vergeet dat ons in 'n moderne en progressiewe wêreld leef waar baie probleme heeltemal oplosbaar is of ten minste reggestel kan word nie. Diabetes mellitus is nie 'n sin nie, en dit is glad nie verbode om lekkers vir diabete te eet nie, maar eers moet u die funksies en nuanses van 'n heerlike dieet bestudeer.
Ja ja! U het goed gehoor: smaaklike dieetkos en selfs soet, wanneer rasioneel gevolg deur wenke, sal die liggaam op geen manier benadeel nie, inteendeel, dit sal u toelaat om die metaboliese prosesse wat versteur word as gevolg van suikersiekte beter aan te pas.
Soet dieet
Ons is gewoond daaraan om die term “dieet” en “dieetkos” te begryp - 'n proses wat gepaard gaan met allerlei pogings uit die wil, die gewete en die beperkings wat ons irriteer, maar dit is nie heeltemal waar nie. In die mediese gemeenskap verwys die term “dieet” na 'n gespesialiseerde voedingskompleks, met 'n lys bykomende aanbevelings en produkte wat die beste by 'n spesifieke siekte pas. Die dieet sluit nie lekkers uit nie en voeg spesiale stowwe by tot die dieet - versoeters en versoeters.
Kan 'n pasiënt met 'n gevestigde diagnose van diabetes iets gebruik? Natuurlik kan dit wel wees, maar hoe dit sy toestand sal beïnvloed, is 'n heeltemal ander kwessie, en waarskynlik sal onbeheerde voeding lei tot die vordering van die siekte, veral as in ag geneem word dat die oorgrote meerderheid pasiënte met diabetes 'n tweede soort siekte het, wat gevorm word as gevolg van 'n onbehoorlike lewenstyl, wanvoeding, en natuurlik 'n predisposisie daarvoor.
Dieet nr. 9 is koolhidraat en is gebaseer op die prestasies van die Amerikaanse dokter Richard Bernstein. Hierdie dieet bevat al die basiese voedselsoorte en bevat baie kalorieë, en dit sluit nie die gebruik van soet vrugte en groente in wat 'n stof soos glukose - sukrose bevat nie, maar maklik verteerbare koolhidrate (suiker, meel) word vervang met versoeters wat nie by koolhidraatmetabolisme ingesluit is nie. Spesiale resepte is ontwikkel vir 'n verskeidenheid heerlike en soet geregte wat met u eie hande berei kan word, en terselfdertyd sal hulle aan die kriteria vir dieet nr. 9 voldoen.
Eenvoudige koolhidrate - skade
Eenvoudige koolhidrate is maklik verteerbare koolhidrate wat amper onmiddellik in die spysverteringskanaal afgebreek word en opgeneem word in die sistemiese sirkulasie. Dit is van eenvoudige koolhidrate wat 'n oplewing in insulienafskeiding voorkom. As 'n pasiënt met hierdie endokriene siekte baie eenvoudige koolhidrate op een slag eet, sal dit 'n skerp toename in bloedglukose veroorsaak. Wat sal lei tot 'n agteruitgang van die welstand. Die mees eenvoudige koolhidraat is suiker.
Eenvoudige koolhidrate bevat ook:
- Bakkery en gebak,
- Lekkers, sjokolade, kakao,
- Sommige vrugte, soos piesang, waatlemoen en spanspek,
- Siroop, konfyt, heuning.
Al hierdie produkte het 'n hoë glukemiese indeks, aangesien dit 'n skerp toename in die konsentrasie van glukose in die bloed skep, wat skadelik is vir enige persoon. Veral vir 'n diabeet. Kan daar diabetes by iemand wees wat voortdurend eenvoudige koolhidrate verbruik? Dit is moontlik, aangesien die risiko vir die ontwikkeling daarvan aansienlik toeneem. Dit is eenvoudige koolhidrate wat aanbeveel word om deur diabete vervang te word met versoeters en versoeters. Dit is belangrik om 'n klein aantekening te maak; lekkers vir diabetici van tipe 1 moet altyd byderhand wees, want met 'n oordosis insulien sal dit help om die newe-effekte van hipoglukemie ontslae te raak.
Komplekse koolhidrate - voordele
Komplekse koolhidrate is 'n kompleks van dieselfde eenvoudige koolhidrate, maar strukturele kenmerke laat sulke molekules nie vinnig af en word in die bloed opgeneem nie. Hulle het nie so 'n soet smaak nie, maar hulle het 'n lae glukemiese indeks en is ideaal vir diabete as hoofdieet.Die smaak van komplekse koolhidrate kan maklik opgelos word deur versoeters wat nie by koolhidraatmetabolisme betrokke is nie, by te voeg.
Wat is soetkoolhidraatvervangers?
Dus, watter lekkers kan mense met diabetes hê? Die moderne farmaseutiese en voedselbedryf staan nie stil nie. 'N Wye verskeidenheid verskillende verbindings wat die soet smaak op smaakknoppies naboots, maar nie koolhidrate is nie, is ontwikkel. Daar is twee hoofgroepe van sulke chemiese verbindings:
Laat ons in meer besonderhede oor elkeen daarvan praat, en ons sal ook die nuttige en skadelike eienskappe van hierdie verbindings verstaan.
Versoeters
Hierdie stowwe bevat koolhidrate, maar het 'n laer kalorie-inhoud as suiker. Versoeters het 'n meer intense smaak en kan met 'n kleiner volume dieselfde smaakeienskappe van 'n gereg hê.
Plaasvervangers bevat stowwe soos:
- Sorbitol is 'n algemene voedingsaanvulling in E420 dieetkos.
- Mannitol - word in plante aangetref en word in die voedselbedryf as voedseladditief E421 gebruik.
- Fruktose - teenwoordig in alle soet vrugte en groente. Dit maak tot 80% heuning by.
- Aspartame is 300 - 600 keer soeter as suiker, ooreenstem met die voedingsaanvulling E951.
'N Waardevolle eienskap van versoeters is 'n ryker smaak in vergelyking met suiker, wat dit toelaat om in baie laer konsentrasies gebruik te word, terwyl die voedselproduk nie die soetheid verloor nie. As versoeters egter opgeneem word, word dit omgesit in glukose en dit verhoog die vlak in die bloed, daarom is dit onmoontlik om dit in groot hoeveelhede te gebruik - dit moet in ag geneem word by diabetes.
Versoeters
Soos suiker en versoeters, het versoeters 'n soet smaak, maar die chemiese struktuur daarvan is glad nie koolhidraat nie. Daar is natuurlike sowel as kunsmatige versoeters. Die natuurlike is: miraculin, osladin, ernandulcin. Tot kunsmatig: sakkarien, siklamaat, neotam. Versoeters het geen kalorie-inhoud nie en word aanbeveel vir gebruik vir tipe 2-diabete en tipe 1-diabete.
Daar is meer as 30 soorte versoeters, waarvan die meeste peptied- of proteïene-aard is. Smaakeienskappe is ook uiteenlopend, van volledige identiteit tot suikers, tot honderde kere beter soetheid. Lekkers vir tipe 2-diabete, wat op versoeters gebaseer is, kan 'n uitstekende plaasvervanger wees vir konvensionele suiker.
Skade deur versoeters en versoeters
Ondanks al die voordele verbonde aan die gebruik van versoeters en versoeters, het die gebruik van hierdie stowwe steeds 'n negatiewe kant. Dus het wetenskaplikes bewys dat met die konstante en oormatige gebruik van suikervervangers sielkundige afhanklikheid ontwikkel. As daar baie versoeters is. Dan ontwikkel daar in die neurone van die brein nuwe assosiatiewe paaie wat bydra tot die skending van die kalorie-waarde van voedsel, veral koolhidraatoorsprong. As gevolg hiervan, lei 'n gebrekkige beoordeling van die voedings eienskappe van voedsel tot die vorming van ooreet, wat die metaboliese prosesse negatief beïnvloed.
Wat is die geheim van die eet van soet diabetes
Alles vernuftig is eenvoudig! Eerstens moet u die vorm van diabetes en die mate van vergoeding vir die manifestasies daarvan ken. Hiervoor is die bepaling van die vlak van geslikte hemoglobien en die beoordeling van die mikrovaskulêre komplikasies van suikersiekte (ondersoek van die fundus by die oogkundige) uitstekend.
Tweedens, as u besluit om geregte met 'n hoë glukemiese indeks te eet, moet u vooraf die hoeveelheid koolhidrate wat in die liggaam binnekom, bereken en dit in broodeenhede (XE) omskakel om die rasionele dosis insulien betyds te bereken.
Derdens kan produkte met 'n hoë glukemiese indeks altyd vervang word met lae-kalorieprodukte met die byvoeging van 'n versoeter, wat u sal bespaar om geëet koolhidrate te bereken en insulien te doseer.
Die ontwikkeling van suikersiekte uit lekkers
Kan diabetes mellitus ontwikkel uit lekkers? Die antwoord op hierdie vraag sal jou ontstel, maar miskien. As die balans tussen voedsel wat verbruik word en gevolglik energie wat daaraan verbonde is en fisieke aktiwiteit nie waargeneem word nie, neem die kans op die ontwikkeling van suikersiekte toe. As u meel, suikergoed en koolzuurhoudende drankies in groot hoeveelhede gebruik, loop u die risiko om vetsug te ontwikkel, wat soms die risiko verhoog om tipe 2-diabetes te ontwikkel.
Wat gebeur as iemand wat oorgewig is hierdie leefstyl voortsit? In die liggaam van so iemand sal stowwe wat die sensitiwiteit van weefsel vir insulien verminder verminder word, en gevolglik sal beta-selle van die pankreas baie meer insulien begin produseer en gevolglik sal die reserwe-produksiemeganismes uitgeput word en die persoon moet insulien terapie gebruik.
Op grond van die inligting wat ontvang is, kan die volgende gevolgtrekkings gemaak word:
- Moenie bang wees vir lekkers nie, u moet net die maatstaf ken.
- As u nie suikersiekte het nie, moet u u liggaam nie tot die uiterste lei nie.
- Vir diabete is daar verskillende alternatiewe vir 'n 'soet' lewe sonder onnodige risiko's. Ons praat oor versoeters, versoeters en 'n rasionele benadering tot die behandeling van diabetes.
Moenie bang wees vir die siekte nie, maar leer om daarmee saam te leef en dan sal u verstaan dat al die beperkings slegs in u kop is!